Инструкции
к практическим работам для 8 класса
Практическая работа 3
Признаки
протекания химических реакций
Цель:
научиться определять по характерным признакам химические явления.
Оборудование:
пробирки, пробиркодержатель, шпатели, пипетка, горелка.
Реактивы:
мел, уксус, крахмал, йодная настойка, сахар.
Ход
работы.
I.
Повторите правила ТБ при работе в химическом кабинете.
Правила
техники безопасности.
1) Внимательно
читайте этикетку на сосуде с тем веществом, которое берете для опыта. Открывая
сосуд с реактивом, не кладите пробку на лабораторный стол боком, а поставьте
вниз дном.
2) Реактивы
берите только в тех количествах, которые указаны в инструкции.
3) Излишек
реактива не сливайте (не высыпайте) назад в посуду, где они находились.
4) Сосуд, из
которого взяли реактив, сразу же закройте пробкой (крышкой) и поставьте на
место.
5) Не
пробуйте вещества на вкус!
6) Будьте
особенно осторожны при работе с нагревательными приборами. Чтобы потушить
горелку, нужно закрыть её колпачком, задувать нельзя.
7) После
окончания работы уберите рабочее место, выключите электронагревательные приборы
и вымойте руки.
Если произошел
несчастный случай, немедленно обращайтесь к учителю.
II.
Ознакомьтесь с инструкцией к практической работе.
Результаты
опытов записывайте в тетрадь сразу же после выполнения опыта.
Опыт 1.
Горение сухого горючего.
Соберите горелку и
зажгите сухое горючее. Что наблюдаете? Потушите горелку с помощью колпачка.
Сделайте вывод о признаке реакции.
Опыт 2.
Взаимодействие крахмала с йодом.
В пробирку
поместите немного порошка крахмала и добавьте каплю йодной настойки. Опишите
наблюдаемые явления. Сделайте вывод о признаке реакции.
Опыт 3.
Нагревание сахара.
В пробирку
поместите немного сахарного песка. Укрепите пробирку в пробиркодержателе.
Зажгите горелку и нагрейте сахар в пробирке. Что наблюдаете? Поставьте пробирку
вместе с держателем в штатив для пробирок. (Ни в коем случае не трогайте
пробирку – она горячая!). Сделайте вывод о признаках реакции.
Опыт 4.
Взаимодействие мела с уксусом.
В пробирку
поместите небольшой кусочек мела и прилейте 1 мл уксуса. Что наблюдаете?
Сделайте вывод о признаке реакции.
III.
Заполните таблицу
|
Описание |
Наблюдения |
Признак |
|
Опыт 1. Зажгли горелку. |
IV. Сделайте
общий вывод к работе.
8 класс
Практическая
работа 6
Решение
экспериментальных задач по теме
«Важнейшие
классы неорганических соединений».
Цель: научиться
решать экспериментальные задачи.
Оборудование:
пробирки.
Реактивы:
в пробирках под номерами растворы кислоты и щелочи; индикаторы (фенолфталеин,
метилоранж), сульфат меди(II), гидроксид натрия, соляная кислота, (для
дополнительной задачи магний, гидроксид магния).
Ход работы
Задача 1. В двух пробирках
находятся растворы кислоты и щелочи. Определите вещества.
Задача 2. Получите гидроксид меди(II) из
имеющихся реактивов.
Задача 3. Химическим способом
отмойте пробирку, загрязненную на практическом занятии гидроксидом меди(II).
Задача 4. В склянке без этикетки
находится бесцветный раствор. Предполагают, что это раствор фенолфталеина.
Проведите опыт, подтверждающий или опровергающий данное предположение.
К задачам 2, 3 и 4 напишите
уравнения реакций.
Напишите вывод к работе.
Дополнительное задание
Задача 5. В вашем распоряжении
магний, гидроксид магния и соляная кислота. Сколькими способами вы сможете
получить хлорид магния?
Практическая работа «Правила ТБ при работе в химическом кабинете. Ознакомление с лабораторным оборудованием».
1. Штатив. Спиртовка.
Рассмотрите штатив и спиртовку. Согласно рисункам, определите их составные части.
2.Соблюдая правила ТБ, подожгите спиртовку. Внимательно рассмотрите её пламя. Аккуратно поднесите одну спичку к нижней, вторую — к средней, третью — к внешней части пламени.
Сделайте выводы, результаты оформите в виде таблицы:
|
Зона пламени |
Цвет пламени |
Характеристика температуры |
Состав |
|
А. Нижняя |
|||
|
Б. Средняя |
|||
|
В. Внешняя |
3. Соберите лабораторный штатив. Закрепите в нём пробирку с водой. При помощи спиртовки нагрейте воду в пробирке.
Дайте письменные ответы на вопросы: А. В какой части пламени следует нагревать пробирку? Почему? Б. Какие правила ТБ необходимо соблюдать для выполнения этого задания?
Практическая работа. Очистка загрязнённой поваренной соли.
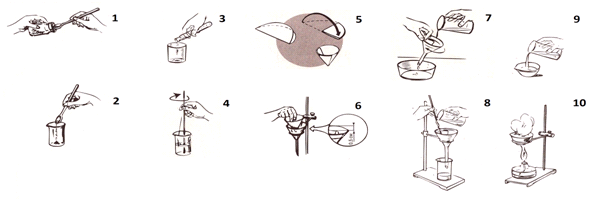
1.Возьмите из банки сухой чистой ложкой загрязнённую поваренную соль. 2. Насыпьте в стакан порцию соли. 3. Добавьте в стакан воды на 1/3 его высоты. 4. Осторожно размешайте содержимое стеклянной палочкой. 5. Приготовьте фильтр как показано на рисунке. 6. Вложите фильтр в воронку так, чтобы он: А) плотно прилегал к стенкам, Б) не доходил до края воронки на 0,5 см. 7. Слегка смочите фильтр водой.
8. Наливайте фильтруемую жидкость на фильтр по стеклянной палочке, направив её нижний конец к стенке воронки, а не в середину фильтра, чтобы не прорвать его. 9. Вылейте фильтрат (раствор соли) в фарфоровую выпаривательную чашку до ½ её объёма. 10. Поставьте чашку на кольцо штатива. Зажгите спиртовку. Нагревайте фильтрат до начала образования кристаллов соли.
11. Оформите в тетради отчёт о работе в виде таблицы:
|
Основные операции (что сделано). |
Рисунки, наблюдения. |
Результаты наблюдений (выводы). |
|
Растворение соли в воде. |
||
|
Фильтрование. |
||
|
Выпаривание фильтрата (раствора соли). |
12. Приведите в порядок своё рабочее место: демонтируйте штатив, разместите на своих местах принадлежности и посуду в чистом виде!
Практическая работа. Получение и свойства кислорода.
1. Соберите прибор как показано на рисунке и проверьте его на герметичность.
В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода.
2. Положите в железную ложечку кусочек древесного угля и раскалите его в пламени. Затем ложечку с тлеющим углём внесите в сосуд с кислородом и наблюдайте за происходящим. Запишите уравнение реакции горения угля (С).
Результаты работы оформите в виде таблицы:
|
Действия (что делали) |
Наблюдения (описание наблюдений) |
Уравнения реакций |
Выводы |
|
1. |
|||
|
2. |
Практическая работа.
Приготовление растворов солей с определённой массовой долей растворённого вещества.
Задача. Приготовьте 100 граммов раствора поваренной соли в воде, с массовой долей соли 20%.
Инструкция:
1. Вычислите, сколько соли и сколько воды потребуется для приготовления данного раствора.
2. Отмерьте на весах необходимую массу соли и поместите её в стаканчик.
3. Отмерьте необходимый объём воды и влейте её в стакан с солью. Содержимое стакана тщательно перемешайте.
Для оформления работы продолжите предложения:
1. Для вычисления массы соли производились следующие расчёты:
2. Для вычисления массы воды производились следующие расчёты:
3. Необходимая масса соли отмерялась с помощью…
4. Необходимый объём (масса) воды отмерялся с помощью…
5. Выводы. Раствор получили путём ….. Растворителем является …. Растворённым веществом…
Практическая работа.
Решение экспериментальных задач по теме
«Основные классы неорганических соединений».
Инструкция
В вашем распоряжении вещества: универсальный индикатор; растворы хлорида натрия, гидроксида натрия, соляной кислоты, хлорида меди (II); металлический магний.
С помощью имеющихся веществ решите экспериментальные задачи:
Задача 1. Даны растворы следующих веществ: хлорид натрия, гидроксид натрия, соляная кислота.
Как опытным путём можно различить эти вещества?
Задача 2. Из металлического магния получите гидроксид магния.
Осуществите превращения: магний → хлорид магния→ гидроксид магния.
Задача 3. Из хлорида меди (II) получите оксид меди (II).
Осуществите превращения: хлорид меди (II) → гидроксид меди(II) → оксид меди(II).
Результаты работы оформите в виде таблицы:
|
Задачи |
Действия |
Наблюдения |
Уравнения реакций |
Выводы |
|
1. |
||||
|
2. |
||||
|
3. |
Литература:
Химия. Неорганическая химия. 8 класс. Учебник для общеобразовательных учреждений. Базовый уровень.
Г.Е. Рудзитис, Ф.Г. Фельдман М.: Просвещение 2015.
В данном комплекте инстукции представлены все инструктивные карточки для проведения химического практикума на уроках химии в 9 классе к учебно-методическому комплексу О.С.Габриеляна. Использование инструктивных карточек позволяет учащимся правильно оформить практические работы, сократить время на оформление, определение плана практической работы. Может быть использован не только при проведении практических работ по химии 9 класса к УМК О.С. Габриеляна, но и при проведении работ к УМК других авторов.
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Практическая работа №1»
Просмотр содержимого документа
«Практическая работа №2»
Просмотр содержимого документа
«Практическая работа №3»
Просмотр содержимого документа
«Практическая работа №4»
Просмотр содержимого документа
«Практическая работа №5»
Просмотр содержимого документа
«Практическая работа №6»
Просмотр содержимого документа
«Практ 2 изменена»
Инструкции
для
выполнения практических работ
по
химии
для
обучающихся 8 классов общеобразовательных
учреждений
(базовый
уровень)
УМК
О.С.Габриелян
Составила
учитель
химии
ГБОУ
«Школа № 15 имени М. С. Батраковой
г.
о. Енакиево»
Толстолуцкая
Елена Ивановна
Практическая
работа № 1
«Правила
работы в лаборатории и приёмы обращения
с лабораторным оборудованием»
Цель
работы:
изучить правила техники безопасности
при работе в химическом кабинете, приемы
обращения с лабораторным оборудованием,
строение пламени.
Реактивы
и оборудование:
лабораторный штатив с лапкой и кольцом,
спиртовка, спички, лабораторная посуда.
Ход
работы
1
Инструктаж по ТБ в кабинете химии.
2
Выполнение практической части работы.
Опыт
1
Знакомство с лабораторным оборудованием
и его назначением.
Опыт
2
Приемы обращения с лабораторным штативом
Лабораторный
штатив служит для закрепления оборудования
во время опытов. Измените положение
лапки и кольца штатива, ослабив винты
и передвинув муфты вдоль стержня.
Закрепите в лапке пробирку вертикально,
затем горизонтально. Помните, что крепко
зажатая пробирка может лопнуть! Сделайте
в тетради рисунок лабораторного штатива.
Подпишите
Опыт
3
Приемы обращения со спиртовкой и изучение
строения пламени.
Зажгите
спиртовку. Изучите части, из которых
состоит пламя. Отметьте цвет пламени.
Потушите спиртовку, накрыв пламя
колпачком. Сделайте в тетради рисунок
спиртовки. Подпишите ее части. Сделайте
рисунок пламени, указав цвет и температуру
пламени.
3
Оформление работы. В тетради для
практических работ начертите таблицу:
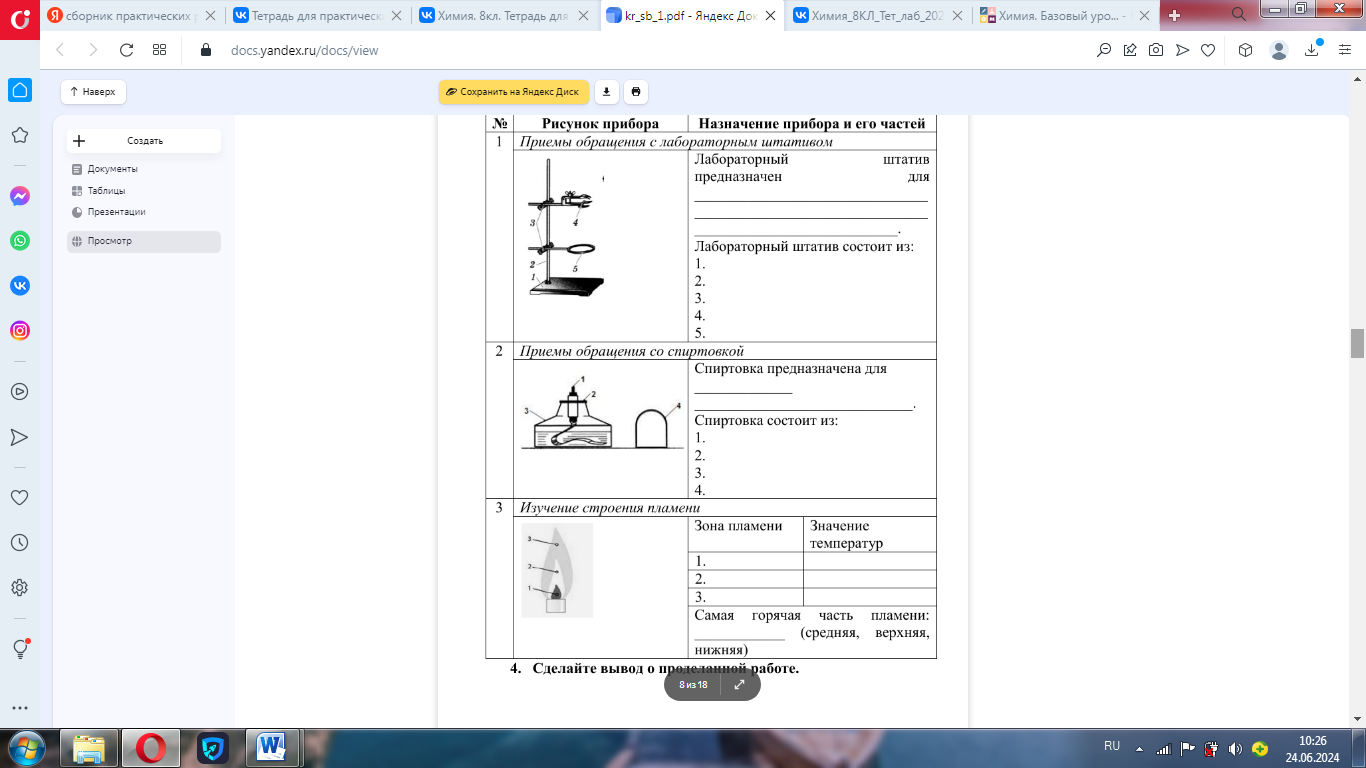
4.
Сделайте вывод о проделанной работе.
Практическая
работа № 2
«Разделение
смесей (на примере очистки поваренной
соли)»
Цель
работы:
изучить простейшие способы очистки
веществ: растворение в воде, фильтрование,
выпаривание.
Реактивы
и оборудование:
спиртовка с поставкой для чаши, спички,
смесь поваренной соли с
песком,
воронка для фильтрования, два химических
стакана, вода, фильтровальная бумага,
фарфоровая чашка для выпаривания,
стеклянная палочка.
Ход
работы
1
Инструктаж по ТБ в кабинете химии.
2
Выполнение практической части работы.
Опыт
1
Растворение в воде
В
стакан со смесью поваренной соли и песка
добавьте воды до половины стакана.
Содержимое стакана перемешайте стеклянной
палочкой. Отметьте изменения, произошедшие
в стакане. Сделайте вывод, для разделения
каких веществ можно применять операцию
растворения в воде.
Опыт
2
Фильтрование
Сложите
бумажный фильтр и поместите в воронку
для фильтрования, предварительно смочив
несколькими каплями воды. Установите
воронку с фильтром на горлышко колбы,
в которую
будет
собираться очищенный раствор (фильтрат).
Медленно тонкой струйкой налейте на
фильтр немного мутного раствора,
полученного в опыте 1. Дождитесь, пока
в колбе соберется
фильтрат.
Отметьте изменения, происходящие на
фильтре. Сделайте вывод, для каких целей
можно применять операцию фильтрования.
Опыт
3
Выпаривание
В
подставку для спиртовки установите
фарфоровую чашку для выпаривания и
поместите в нее 1 мл фильтрата. Зажгите
спиртовку и продолжайте нагревание до
полного испарения жидкости на предметном
стекле. Отметьте изменения, происходящие
на предметном стекле. Сделайте вывод,
для каких целей можно применять операцию
выпаривания.
3.
Оформление работы
Результаты
выполнения работы записывают в таблицу:
|
№ и |
Что |
Что |
Выводы |
4.
Сделайте общий вывод о выполненной
работе.
5.
Выполните тестовые задания
1.
Отличие морской соли от поваренной в
том, что первая:
А)
не растворяется в воде; Б) не солёная
на вкус; В) содержит много примесей;
Г) другое химическое вещество.
2.
Какими физическими свойствами не
обладает соль?
А)
солёная; Б) плохо растворяется в воде;
В) имеет белый цвет; Г) сыпучий порошок.
3.
Какой метод можно использовать для
очистки поваренной соли?
А)
фильтрование; Б) кристаллизация; В)
выпаривание; Г) хроматография.
4.
Какую смесь можно разделить методом
фильтрования?
А)
сахара и песка; Б) соли и сахара; В)
железных опилок и древесной стружки;
Г) бензина и воды.
5.
Что из перечисленного является эмульсией?
А)
растительное масло; Б) раствор соли;
В) майонез; Г) чай.
Практическая
работа № 3
«Получение
и собирание кислорода, изучение его
свойств»
Цель
работы:
получить кислород методом вытеснения
воздуха и методом вытеснения водой и
изучить его свойства.
Реактивы
и оборудование:
пероксид водорода, оксид марганца,
лучина, пробка с газоотводной трубкой,
лучинка, спиртовка, спички, химический
стакан, вата, пробирка.
Ход
работы:
1
Инструктаж по ТБ в кабинете химии.
2
Оформление практической работы:
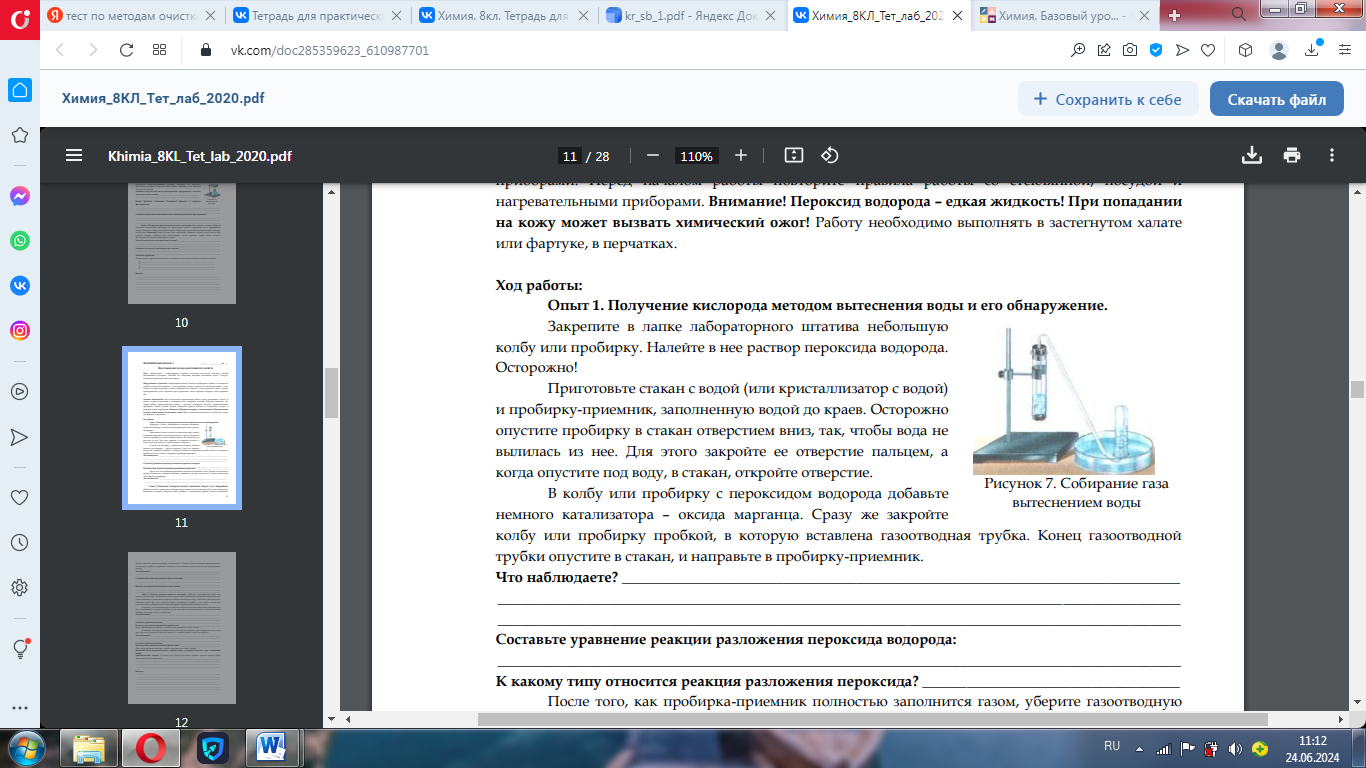
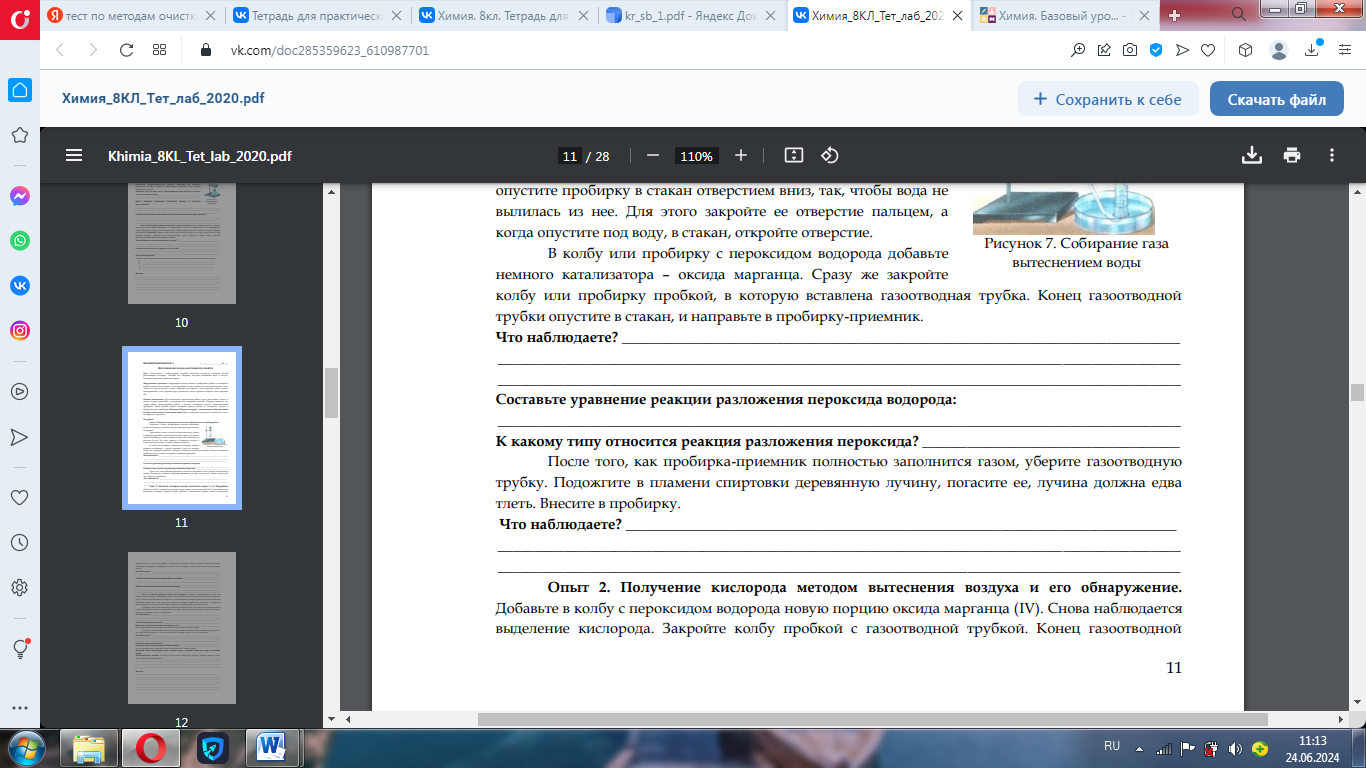
3.
Оформление работы
Результаты
выполнения работы записывают в таблицу:
|
№ и |
Что |
Что |
Выводы |
4.
Сделайте вывод о проделанной работе,
ответив на вопросы:
1
Из каких веществ получают кислород в
лаборатории? 2 Как доказать, что полученный
газ — кислород? 3 Какие вещества называются
катализаторами?
Практическая
работа № 4
«Получение
и собирание водорода, изучение его
свойств»
Цель:
получить водород в лаборатории и изучить
его свойства.
Оборудование
и реактивы:
цинк, соляная кислота, лучина, спички,
газоотводная трубка, две пробирки,
штатив.
Ход
работы:
1
Инструктаж о правилах техники безопасности.
2
Выполнение практической работы.
Опыт
№ 1
Получение водорода реакцией замещения
между цинком и соляной кислотой.
В
пробирку опустите 2-3 гранулы цинка.
Налейте
соляной кислоты (столько, чтобы кислота
лишь покрывала цинк) и закройте пробкой
с газоотводной трубкой. Газоотводную
трубку накройте чистой пробиркой.
Пронаблюдайте
за происходящим в пробирке.
Опыт
№ 2
Изучение физических свойств водорода.
Рассмотрите
пробирку с собранным водородом и отметьте
его физические свойства: агрегатное
состояние, цвет, запах, растворимость
в воде, плотность по отношению к воздуху.
Запишите
название опыта, ваши наблюдения и
соответствующий вывод.
Опыт
№ 3
Проверка водорода на чистоту.
Для
опыта используется водород, собранный
вытеснением воздуха. Не изменяя положения
пробирки приемника, поднесите ее вплотную
к пламени горелки или спички и резко
поверните так, чтобы ее отверстие
оказалось в пламени. Если при этом
раздается резкий “лающий” звук, с газом
(водородом) работать нельзя, так как он
содержит примесь воздуха. Необходимо
некоторое время подождать, пока из
пробирки будет вытеснен весь воздух.
Если вы услышите легкий звук, напоминающий
“п-пах”, с водородом можно работать.
Запишите название опыта, ваши наблюдения
и соответствующий вывод.
3.
Оформление в виде таблицы:
|
№ и |
Что |
Что |
Уравнения |
|
|||
|
|||
|
4.Сделайте
вывод о проделанной работе.
5.
Выполните тестовые задания.
1.
Агрегатное
состояние водорода при нормальных
условиях
а)
жидкость б) твердое вещество
в) газ
2.
Формула
простого вещества водорода
а)
Н3
б) Н 2
в) Н
3.
Водород
в лаборатории получают реакцией
а)
Zn + HCl б) CH4 +
H2O
в) H2O
+ C
4.Группа,
в которой находится водород
а)
3 б) 2
в) 1
5.
Порядковый
номер водорода
а)
1 б) 2
в) 3
Практическая
работа № 5
«Приготовление
растворов с определённой массовой долей
растворённого вещества»
Цель:
применение приобретенных навыки по
решению задач на приготовление растворов
для приготовления раствора с определенной
массовой концентрацией; продолжить
формировать навыки обращения с
лабораторным оборудованием, посудой,
химическими реактивами.
Оборудование
и реактивы:
весы, стаканы, стеклянная палочка,
шпатель, мерный цилиндр или мензурка,
хлорид натрия.
Ход работы:
1
Инструктаж о правилах техники безопасности.
2
Выполнение практической работы.
Шаг 1.
Рассчитайте массу хлорида натрия и
объем воды, необходимые для приготовления
раствора массой ____________ г, с массовой
долей растворенной соли ___________% (данные
для задачи указывает учитель).
Дано:
m(раствора)
= г Решение:
ω (NaCl) = %
Ответ:
m(NaCl) — ? V(H2O) — ?
Шаг 2.
При помощи весов взвесьте рассчитанное
количество хлорида натрия. Навеску соли
аккуратно перенесите в стакан.
Шаг 3.
Отмерьте необходимый объем воды при
помощи мерного цилиндра или мензурки.
Шаг 4.Прилейте
отмеренный объем воды к навеске соли в
стакане. Размешайте смесь палочкой до
полного растворения соли.
3 Сделайте
вывод о проделанной работе.
4. Ответьте
на контрольные вопросы:
1). Какое
вещество называют растворителем?
2). Как изменится
массовая доля приготовленного вами
раствора, если его разбавить водой в
два раза?
3). Какие
растворы называются насыщенными?
Практическая
работа № 6.
Решение
экспериментальных задач по теме «Основные
классы неорганических соединений»
Цель:
закрепить знания об основных классах
неорганических соединений, научиться
решать экспериментальные задачи.
Оборудование
и реактивы:
магний, оксид магния, растворы: HCl, NaOH,
CuSO4; индикаторы, пипетка, стеклянная
палочка.
Ход
работы:
1
Инструктаж по правилам ТБ при работе в
кабинете химии.
2
Ознакомьтесь с заданием:
Задание
1
В двух пробирках находятся растворы: в
1 – раствор соляной кислоты, во 2-
гидроксида натрия. Как опытным путем
определить, в какой пробирке находится
каждое из веществ?
Задание
2
В вашем распоряжении есть магний, оксид
магния и кислоты. Получить хлорид магния.
Задание
3
Осуществите превращения по схеме: CuSO4
→ Cu(OH)2.
3
Выполните необходимые опыты.
4
Результаты проведенной работы оформите
в виде таблицы:
|
№ опыта |
Что |
Что |
Уравнения |
|
|
Стеклянной полоску индикатора пробирок, приливаем |
||
|
|
соляной опускаем немного |
||
|
|
сульфата |
5
После проведения практической работы
сделайте общий вывод.
Практическая работа №3: «Очистка загрязненной воды».
Цель работы: овладеть простейшими способами очистки воды от примесей: путем фильтрования, кипячения и перегонки (дистилляции).
Оборудование: Лабораторный штатив с кольцом, два химических стакана, воронка, фарфоровая чашка, готовый фильтр, стеклянная палочка с резиновым наконечником, шпатель, спиртовка, спички, загрязненная речным песком и илом вода.
Примечание: Вспомни правила поведения и техники безопасности процессов фильтрования, нагревания, выпаривания. Внимательно слушай указания учителя.

Весь материал — смотрите архив.
