Титрованные растворы
готовят также из точно отвешенного
количества вещества, запаянного в
стеклянные ампулы, называемые фиксаналами,
необходимого для приготовления 1 л
титрованного раствора.
С ампулы снимают
этикетку, обмывают дистиллированной
водой. В однолитровую мерную колбу
вставляют стеклянную воронку, в которую
помещают прилегаемый к фиксаналу
стеклянный боек. Держа ампулу над
воронкой, разбивают ударом об острие
бойка нижнее углубление, затем стеклянной
острой палочкой пробивают верхнее
углубление ампулы, отчего содержимое
ампулы попадает в колбу. Тщательно
промывают внутренность ампулы
дистиллированной водой, стекающей в ту
же колбу. Ампулу выбрасывают, а колбу
доливают дистиллированной водой до
метки и тщательно перемешивают раствор.
В фиксанале
содержится обычно 0,1 грамм-эквивалента
вещества, так что при растворении в 1 л
получается децинормаль-ный раствор.
При необходимости другой концентрации
содержимое ампулы разводят в колбе
другой емкости.
14. Прямое, заместительное и обратное титрование.
Титрование можно
выполнить различными способами. И
поэтому разли-
чают: прямое,
обратное и заместительное титрование.
Прямое титрование
– к раствору определяемого вещества
до-
бавляют небольшими
порциями титрант (рабочий раствор).
Определяемое
вещество непосредственно реагирует с
титрантом.
Обратное титрование
– используют два титранта. Сначала к
анализи-
руемому раствору
добавляют избыток одного титрованного
раствора – ти-
ранта-1. Не
прореагировавший титрант-1 оттитровывают
другим
стандартным
раствором – титрантом-2. Количество
израсходо-
ванного титранта-1
на взаимодействие с определяемым
веществом опреде-
ляют по разнице
между добавленным объемом (V1 ) и объемом
(V2 ), пошед-
шим на титрование
титранта-2.
Заместительное
титрование
– применяют в тех случаях, когда прямое
или обратное
титрование вещества невозможно или
вызывает затруднение,
т.е. непосредственная
реакция исследуемого вещества и реагента
не удовле-
творяет требованиям,
предъявляемым к реакциям, применяемым
в титримет-
рии. К определяемому
веществу добавляют какой-либо реагент,
при взаимо-
действии с которым
количественно выделяется продукт
реакции. А затем
продукт реакции
титруют подходящим титрантом.
15. Титрование по методу отбора аликвоты и по методу отдельных навесок
В объемном анализе
титрование можно проводить 2 способами:
1) метод пипетирования
2) метод отельных
навесок
В первом случае
калиброванной пипеткой отбирают аликвоту
– точно измеренный V
р-ра, содержащего определенную часть
анализируемого вещества и титруют эту
аликвоту.
Во втором случае
берут отдельные близкие по величине
навески анализируемого вещ-ва, растворяют
каждую навеску в произвольном объеме
воды и затем титруют целиком приготовленный
раствор.
16. Кислотно-основное титрование или метод нейтрализации: теоретические основы, кислотно-основные индикаторы.
Кислотно-основной
метод анализа основан на реакции, при
которой происходит связывание катионов
H+
с OH—
(ионами гидроксида). Образуются молекулы
воды (H2O)
и, следовательно, при титровании
происходит изменение pH раствора.
Кислотно-основные
методы делят на 2 вида анализа:
алкалиметрию
ацидиметрию
Алкалиметрия — в
данном анализе стандартным раствором
является раствор щелочи: KOH, NaOH. Его
готовят в приближенной концентрации,
а точную концентрацию устанавливают
по щавелевой кислоте или раствору KOH
известной концентрации. Этим методом
определяют содержание кислот, солей
слабо гидролизующихся и сильных кислот.
Ацидиметрия —
стандартным раствором является раствор
кислоты, который готовят в приближенной
концентрации, а точную концентрацию
устанавливают по химически чистым
веществам Na2B4O7·10H2O, или Na2CO3. Данным
методом определяют в исследуемых
растворах содержание щелочей, солей,
сильно гидролизуемых и слабых кислот
(подвергающихся гидролизу, имеющих
щелочную среду), оксидов (CaO, BaO, MgO), а
также карбонатную жесткость воды.
По ходу
кислотно-основного титрования изменяется
концентрация H+ и OH-, следовательно
изменяется и pH титруемого раствора. При
определенных значениях pH достигается
точка эквивалетности и титрование в
этот момент заканчивается.
Индикаторами в
методе кислотно-основного титрования
служат вещества, меняющие свою окраску
при изменении рН среды. Поэтому их
называют кислотно-основными, или
рН-индикаторами. Наиболее широко
используются в анализе: метиловый
оранжевый, фенолфталеин, лакмус, метиловый
красный, тимолфталеин, бромтимоловый
синий.
Приготовление растворов из фиксаналов
Точные растворы можно быстро приготовить используя для этого фиксаналы. Фиксанал представляет собой точно отвешенную массу вещества или его раствора, запаянного в стеклянную ампулу. Фиксанал продается в коробках по 10 ампул. На каждой ампуле имеется штемпель или этикетка с обозначением формулы находящегося в ампуле вещества и его количества — 0,1 или 0,01 экв. При количественном перенесении содержимого ампулы в мерную колбу и разбавлении его до 1 л получают точно 0,1 или 0,01 н. раствор.
Для приготовления раствора сначала удаляют теплой водой штемпель (или этикетку) с ампулы, затем ополаскивают ее дистиллированной водой. В обычную химическую воронку помещают коротким острым концом вверх боек с крестовидным утолщением, который обычно прилагается к каждой коробке фиксанала. Воронку с бойком вставляют в горло мерной колбы вместимостью 1 л. Затем дно ампулы разбивают осторожным ударом об острый конец бойка, после чего пробивают вторым бойком боковое или верхнее углубление ампулы.
Содержимое ампулы тщательно вымывают струей воды из промывалки в мерную колбу. Вещество в колбе растворяют в воде и доводят объем раствора до метки. Колбу закрывают пробкой и раствор хорошо перемешивают.
Фиксаналы едких щелочей могут храниться до 6 месяцев, так как при более длительном хранении реактивы загрязняются продуктами выщелачивания стекла. Фиксаналы солей и кислот могут храниться неограниченное время.
При пользовании фиксаналом 0,1 н. йодида необходимо перед вскрытием ампулы поместить в мерную колбу 30-40 г иодида калия. Если ампула содержит 0,01 эквивалента йода, то добавка йодида калия не требуется. Для растворения вполне достаточно того количества йодида калия, которое имеется в ампуле. Содержимое ампулы можно растворить в мерной колбе вместимостью 100 мл или 1 л для получения соответственно 0,1 или 0,01 н. раствора йода.
Фиксаналы дают возможность быстро готовить 0,1 или 0,01 н. растворы в экспедиционных условиях.
Выпускают фиксаналы следующих веществ:
H2SO4; HCl; NaOH; KOH; Na2CO3; NaHCO3; NaCl; Na2C2O4; H2C2O4-2H2O; K2Cr2O7; K2CrO4; Na2S2O3-5H2O; KMnO4; NH4SCN; KSCN; K2C2O4; NaSCN; BaCl2-2H2O; (NH4)2C2O4-H2O; J2; Na2B4O7-10H2O; KCl; KJ; NH4Cl; K2CO3; KJO3; AgNO3.
Содержание
Приготовление растворов:
- из твердых веществ
- щелочей и кислот
- из фиксаналов
Приготовление растворов из твердых веществ
Количество твердого вещества, которое можно растворить в данном количестве воды, имеет предел, зависящий от свойств взятых веществ и от тех условий, в которых происходит растворение. Когда этот предел достигнут, получается насыщенный раствор. Концентрация насыщенного раствора называется растворимостью.
Следовательно, насыщение раствора каким-либо веществом зависит от его растворимости в данном растворителе при данных условиях. Таким образом, совершенно не обязательно, чтобы концентрация насыщенного раствора была бы высокой.
Растворимость твердого вещества можно повысить, если раствор нагревать. Однако некоторые соли не подчиняются этому правилу. Растворимость их или понижается с повышением температуры или повышается только до определенной температуры, выше которой растворимость уменьшается. Скорость растворения твердого вещества зависит от размера его частиц. Чем крупнее куски, тем медленнее идет растворение; наоборот, чем мельче отдельные частицы твердого вещества, тем скорее переходит оно в раствор. Поэтому перед растворением твердого вещества его всегда следует измельчить в ступке и отвешивать для растворения только измельченное вещество. Сказанное не относится к гигроскопичным веществам, так как последние в измельченном виде очень легко поглощают влагу из воздуха вследствие большого увеличения поверхности. Поэтому гигроскопичные вещества растворяют, не измельчая, разве только быстро разбив большие куски.
Иногда при растворении твердых веществ, например кристаллических, их помещают в колбу. При неправильном введении таких веществ (особенно крупных кусков или кристаллов) случается, что колба разбивается. Чтобы не разбить колбу, поступают так: наклоняют ее под углом не больше 45° (лучше меньше) и опускают твердое вещество, чтобы оно скатывалось по горлу и стенке шара колбы. Удобнее сначала налить в колбу часть рассчитанного количества растворителя, например воды, а затем вводить твердое вещество, как описано выше, иногда встряхивая колбу. Оставшуюся часть растворителя вводят после того, как будет пересыпано все количество твердого вещества, предназначенного для растворения.
Вернуться к содержанию
Приготовление растворов щелочей и кислот
При растворении щелочей в воде происходит сильное разогревание, поэтому для приготовления таких растворов следует пользоваться не стеклянными, а фарфоровыми сосудами. Раствор перемешивают стеклянной палочкой. Нужно следить, чтобы брызги раствора ни в коем случае не попали в глаза, на кожу и одежду.
Концентрированные растворы щелочей выщелачивают стекло, поэтому лучше хранить эти растворы в полиэтиленовой посуде или в стеклянной бутыли, внутренние стенки которой предварительно покрывают парафином.
При разбавлении кислот необходимо приливать кислоту к воде, а не наоборот. Смешивание кислоты с водой сопровождается сильным разогреванием, поэтому при добавлении воды в кислоту происходит разбрызгивание кислоты, что очень опасно. Если кислота попала на кожу или одежду, необходимо смыть ее большим количеством воды, а затем нейтрализовать раствором щелочи.

Рис. 1. Техника безопасности при приготовлении растворов концентрированных кислот
1 – нельзя добавлять воду в кислоту; 2 – при смешивании кислоты и воды происходит выделение большого количества тепла; 3 – раствор может вскипеть и выплеснуться из емкости; 4 – приливайте кислоту к воде при постоянном перемешивании.
Растворы кислот хранят в плотно закрытых сосудах.
Вернуться к содержанию
Приготовление растворов из фиксаналов
Для быстрого приготовления точных растворов пользуются фиксаналами.
Фиксанал – точно взвешенное количество реактива, необходимое для приготовления 1 литра 0,1 н или 0,01 н растворов, содержащееся в запаянной стеклянной ампуле. Количество вещества в ампуле соответствует определенному числу грамм-эквивалентов данного вещества, и при растворении его образуется раствор известной нормальности. Фиксанал может быть в виде навески твердого вещества или в виде точно отмеренного объема раствора.
Для приготовления раствора из фиксанала содержимое ампулы количественно переносят в мерную колбу и раствор разбавляют дистиллированной водой, доводят его объем до метки:
1. Ампулу обмывают сначала теплой, а затем холодной дистиллированной водой, чтобы смыть этикетку и возможные загрязнения.
2. Перед приготовлением раствора один из бойков (крестовидный), находящийся в коробке с фиксаналом, обливают сначала водопроводной, а затем дистиллированной водой. Боек помещают в чистую воронку таким образом, чтобы длинный конец его был вставлен в трубку воронки, а короткий острый конец — направлен кверху; крестовидное утолщение бойка упирается в нижнюю часть конуса воронки.
3. Воронку вместе с бойком вставляют в чистую мерную колбу.
4. Ампулу переворачивают дном книзу и, ударяя ее нижним углублением по бойку в воронке, разбивают дно ампулы. Не изменяя положения ампулы над воронкой, вторым бойком пробиваю верхнее углубление на ней. Содержимое ампулы при этом выливается или высыпается в мерную колбу.
5. Ампулу держат в том же положении и в образовавшееся верхнее отверстие вставляют конец трубки промывалки и сильной струей воды из промывалки хорошо промывают наружную поверхность ампулы и воронку с бойком, после чего воронку вынимают из колбы.
6. Уровень жидкости в колбе доводят до метки. Колбу плотно закрывают пробкой и тщательно перемешивают раствор.
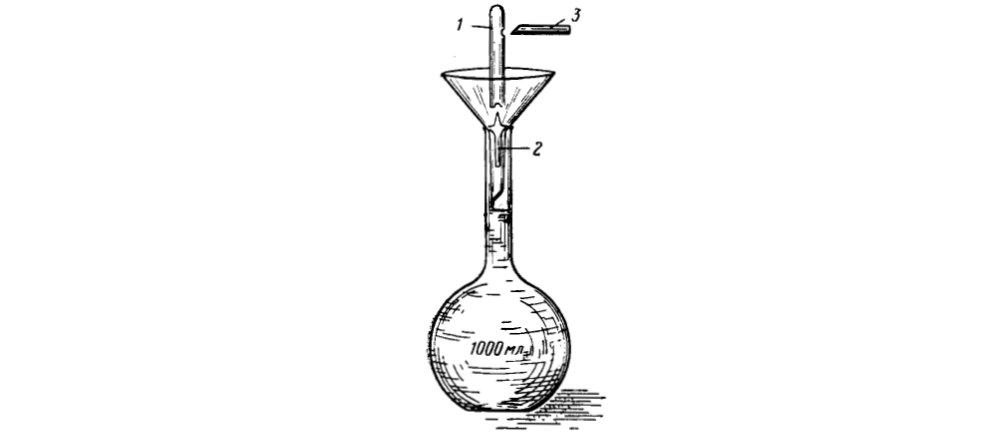
Рис. 2. Перенос содержимого ампулы фиксанала в мерную колбу
1 – ампула с точной навеской вещества; 2 – крестовидный боек; 3 – боек для стенки ампулы.
Подробнее о способах приготовления растворов по точной и приблизительной навеске, расчете концентрации полученного раствора и установке титра читайте в статье «Способы приготовления растворов».
Вернуться к содержанию
Ссылка на источник
Титриметрический анализ основан на точном измерении объема стандартного раствора реагента (титранта), израсходованного на реакцию с определяемым веществом.
Раствор титранта должен быть стандартизирован. Под стандартизацией раствора титранта понимают установление его точной концентрации с относительной погрешностью, обычно не превышающей 0,1 %.
Расчет результатов титриметрического анализа основан на принципе эквивалентности, в соответствии с которым вещества реагируют между собой в эквивалентных количествах.
Существуют методы прямого, обратного (титрования по остатку) титрования и титрования по замещению.
При прямом титровании определяемое вещество реагирует с титрантом, и для проведения анализа этим методом достаточно одного стандартного раствора.
В методах обратного титрования используют два стандартных раствора – основной и вспомогательный. Широко известно обратное титрование хлорид-иона в кислых растворах. К анализируемому раствору хлорида сначала добавляют заведомый избыток титрованного раствора нитрата серебра (основного стандартного раствора). При этом происходит реакция образования малорастворимого хлорида серебра. Не вступившее в реакцию избыточное количество нитрата серебра оттитровывают раствором тиоцианата аммония – вспомогательного стандартного раствора. Количество хлорида легко рассчитать, так как известны количества нитрата серебра, введенного в раствор и не вступившего в реакцию с хлоридом.
В методе титрования по замещению к определяемому веществу добавляют избыток специального реагента, вступающего в реакцию с определяемым веществом. Один из продуктов взаимодействия, количество которого эквивалентно количеству определяемого вещества, оттитровывают затем стандартным раствором.
В титриметрическом (объемном) анализе основным методом является титрование. Титрованием называется процесс добавления из бюретки каплями раствора известной концентрации к раствору определяемой концентрации до достижения точки эквивалентности, которую устанавливают при помощи индикатора или прибора. Титрованные (стандартизированные) растворы – это растворы точно известной концентрации, выраженной в титрах. Титр раствора – это количество вещества в граммах, содержащееся в 1 см3 раствора.
В зависимости от способа приготовления различают титрованные растворы приготовленные и установленные.
Приготовленные растворы. Соединения, состав которых строго соответствует химической формуле, химически чистые, устойчивые при хранении (как в твердом виде, так и в растворе) обладают большой молярной массой эквивалента. Их называют стандартными исходными веществами (первичными стандартами) для установки титра других рабочих растворов. Нужная навеска стандартного вещества (G, г) в соответствии с заданной нормальностью и объемом раствора равна
G = V • N • Э,
где V – объем раствора, см3; N – нормальность раствора; Э – грамм-эквивалент вещества.
Навеску отвешивают на аналитических весах в весовом стаканчике (бюксе) с точностью до 0,0002 г, переносят в мерную колбу определенной вместимости, смывая навеску со стенок стаканчика и воронки небольшим количеством растворителя, растворяют (количество растворителя до 1/3 вместимости колбы), выдерживают 0,5 ч в термостате при 20 °С, а затем объем раствора доводят до метки и тщательно перемешивают. В этом случае титр раствора (Т, г/см3) равен навеске (G, г), деленной на объем раствора (V, см3): Т = G / V.
Чтобы перейти к нормальности N, достаточно титр раствора умножить на 1000 и разделить на грамм-эквивалент растворенного вещества (Э)
N = 1000 • Т / Э.
Пример. Если навеску карбоната натрия Na2СО3 массой 1,0621 г растворили в мерной колбе вместимостью 100 см3, то титр раствора Т = 1,0621/100 = 0,010621 г/см3, а нормальность раствора N = (0,010621 • 1000)/53 = 0,2004.
Титрованные растворы, полученные из точной навески вещества, называют приготовленными.
Стандартными веществами для установления титра растворов кислот служат тетраборат (Nа2В4О7 • 10Н2О) и карбонат натрия (Nа2СО3), щелочей – щавелевая (Н2С2О4 • 2Н2О) и янтарная [СО2Н(СН2)2СО2Н)] кислоты.
Растворением навески исходного вещества получают стандартный раствор для установки титра рабочих растворов.
Приготовляя титрованный раствор из навески, не стремятся получить строго определенную нормальность (или титр), а вычисляют поправку к нормальности раствора.
Пример. При приготовлении 100 см3 0,1 н раствора, взяли навеску карбоната натрия (Na2СО3) 0,5308 г. Теоретически рассчитанная навеска в этом случае должна быть равна 0,5300 г. Тогда поправочный коэффициент будет иметь следующую величину:
к = взятая навеска / рассчитанная навеска = 0,5308 / 0,5300 – 1,00151.
Следовательно, приготовленный раствор в 1,00151 раза концентрированнее строго децинормального.
Поправочный коэффициент иначе называют фактором нормальности или просто поправкой к нормальности раствора.
Установленные растворы (вторичные стандарты). В качестве рабочих титрованных растворов чаще всего используют минеральные кислоты, щелочи, перманганат калия, тиосульфат натрия (гипосульфит). Все эти вещества не удовлетворяют требованиям, предъявляемым к стандартным веществам (их точные растворы нельзя готовить из навески). Поэтому приблизительные количества таких веществ (навеска взвешивается на технических весах или отмеряется мерным цилиндром) растворяют в необходимом объеме воды и титруют раствором подходящего стандартного вещества (первичного стандарта). По затраченным объемам и известной концентрации исходного раствора вычисляют нормальность и титр устанавливаемого раствора. Так, нормальность раствора едкого натра устанавливают по стандартному раствору щавелевой кислоты, а нормальность соляной кислоты – по исходному раствору тетрабората натрия.
Растворы, титр которых находят не по точной навеске, а устанавливают по тому или иному стандартному веществу, называют установленными или стандартизированными.
Этот метод очень удобен, так как при нем не требуется устанавливать титр каждого рабочего раствора по исходному веществу. Любой стандартный раствор дает возможность последовательно установить титры всех необходимых рабочих растворов, однако он менее точен, так как при этом суммируются погрешности, допускаемые в процессе установки отдельных титров, и поэтому приготовление исходного титрованного раствора всегда требует особой тщательности. Чтобы уменьшить погрешности, титр рабочего титрованного раствора устанавливают, по возможности, в таких же условиях, какие будут при выполнении анализа. Для установки титра и выполнения анализа следует пользоваться одной и той же мерной посудой (предварительно прокалиброванной).
Если титрованный раствор используют при разной температуре, то следует вводить температурную поправку. Изменение температуры на 10 ºС изменяет k на 0,02.
При стандартизации растворов используют методы отдельных навесок и пипетирования.
Метод отдельных навесок. Рассчитывают навеску стандартного вещества исходя из того, что на ее титрование будет израсходовано 18…20 см3 титранта. На аналитических весах «методом отсыпания» отмеряют три навески. Для этого взвешивают чистый сухой бюкс с такой массой анализируемого вещества, которая достаточна для трех навесок, и записывают его массу. Затем снимают бюкс с весов и легким постукиванием указательного пальца правой руки отсыпают примерно третью часть содержимого в коническую колбу. Бюкс при этом располагают над центром горлышка колбы. После этого возвращают его в вертикальное положение и вновь взвешивают. Если навеска меньше требуемой, повторным отсыпанием добиваются, чтобы она была в указанных пределах. Навеску выше рассчитанной отбрасывают, колбу моют и навеску берут заново.
В каждую колбу приливают приблизительно по 20 см3 дистиллированной воды, перемешивают до полного растворения стандартного вещества, вводят 1…2 капли индикатора и титруют. По бюретке делают отсчет объема стандартизируемого раствора и записывают в журнал. Рассчитывают молярную концентрацию титранта для каждой навески стандартного вещества и расхождение между наибольшим и наименьшим результатами (в %). Если расхождение не превышает 0,2…0,3 %, то берут среднее значение из трех результатов. В случае большего расхождения взвешивают еще одну навеску стандартного вещества, титруют ее, находят четвертый результат и снова проверяют сходимость значений молярной концентрации.
Метод пипетирования. Рассчитывают навеску стандартного вещества, необходимую для приготовления заданного объема раствора первичного стандарта концентрации (как правило, близкой к молярной концентрации титранта). Взвешенную на аналитических весах навеску количественно переносят в мерную колбу через воронку, смывая навеску из стаканчика струей воды из промывалки. По окончании растворения объем раствора доводят до метки и перемешивают. Аликвоту (определенную часть 1/5, 1/10 и т. д.) полученного раствора отбирают пипеткой, предварительно ополоснутой этим раствором. При стандартизации раствора титрование проводят не менее трех раз. Если объемы, затраченные на титрование, совпадают между собой в пределах 0,2…0,3 %, то берут среднее значение и рассчитывают молярную концентрацию титранта. В случае большого расхождения проводят повторное титрование.
В практике технического анализа титрованные растворы приготовляют из фиксаналов или стандарт-титров. Фиксанал – это количество вещества в запаянной стеклянной ампуле, необходимое для приготовления 1 дм3 точно 0,1 н или 0,01 н раствора. Промышленно выпускаются фиксаналы с различными рабочими веществами как в виде растворов (серная и соляная кислота, едкий натр и едкое кали), так и сухие (перманганат калия, карбонат или оксалат натрия и др.). В каждой коробочке с фиксаналами имеется стеклянный боек и стеклянная палочка.
Содержимое ампулы количественно переносят в мерную колбу вместимостью 1 дм3 (или 0,5 дм3, если это указано специально) и доводят водой до метки. Для этого в горлышко колбы вставляют воронку и вкладывают стеклянный боек, о который и разбивается дно ампулы. Затем стеклянной палочкой пробивают отверстие в верхней части ампулы и дают содержимому ее полностью вытечь или высыпаться (рис. 2.12) в колбу. Через образовавшееся отверстие ампулу и воронку тщательно ополаскивают водой и доводят объем раствора в колбе до метки.
Рис. 2.12. Приготовление рабочего раствора из фиксанала
При правильном хранении рабочие титрованные растворы служат несколько месяцев, не изменяя своей концентрации. Особенно тщательной защиты от диоксида углерода воздуха требуют растворы щелочей.
Склянки, в которых хранятся рабочие растворы, обычно соединяют с бюреткой посредством сифона (рис. 2.13). Это позволяет наполнять бюретку, не загрязняя раствор.
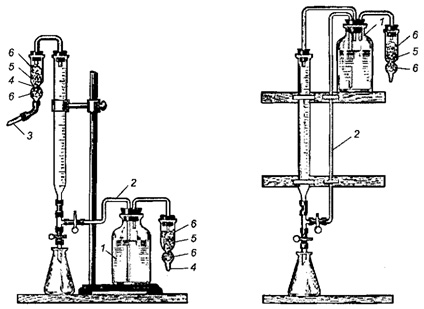
Рис. 2.13. Два способа соединения бюретки со склянкой, содержащей запасной раствор:
1 – склянка с запасным раствором; 2 – сифон для переливания раствора в бюретку; 3 – трубка для засасывания раствора;
4 – трубка для натронной извести; 5 – натронная известь; 6 – вата
Для определения концентрации установленных растворов приготовляют определенный объем раствора с приблизительной нормальностью, а затем по результатам титрования устанавливают точную нормальность.
Пример. Необходимо приготовить 300 см3 приблизительно 0,2 н раствора Н2SО4 из кислоты плотностью 1,84 г/см3 при 20 ºС и установить точную нормальность по рабочему раствору NaОН.
При полной нейтрализации серной кислоты грамм-эквивалент ее равен 98,08 : 2 = 49,04 г. Поэтому количество чистой Н2SО4 необходимое для приготовления 0,3 дм3 приблизительно 0,2 н раствора будет 49,04 • 0,2 • 0,3 = 2,9424 г.
Серная кислота плотностью 1,84 г/см3 имеет концентрацию 96,0 %. Легко вычислить, в каком количестве этой кислоты содержатся 2,9424 г чистой Н2SО4.
100 г 96%-ной кислоты содержат 96 г Н2SО4
х г 96 %-ной кислоты 2,9424 Н2SО4
х = (100 • 2,9424) / 96 = 3,065,
что соответствует объему кислоты 3,065/1,84 = 1,67 см3.
Таким образом, для приготовления 300 см3 приблизительно 0,2 н раствора серной кислоты нужно взять 1,67 см3 концентрированной серной кислоты (плотность 1,84 г/см3).
Действительную нормальность этого раствора устанавливают по исходному веществу (Na2СО3, Na2В4О7 • 10Н2О) или по точному раствору едкого натра путем титрования. Используя уравнение N1V1 = N2V2, вычисляют нормальность растворов по результатам титрования.
Допустим, что нормальность серной кислоты устанавливали по титрованному раствору щелочи. При этом на 10 см3 0,112 н. раствора NaОН израсходовали в среднем 10,08 см3 кислоты. Тогда
NH2SO4 • 10,08 = 0,112 • 10,00;
NH2SO4= 0,112 • 10,00 / 10,08 = 0,111.
Точность титриметрических определений. Операции титриметрического анализа выполняются с некоторыми, хотя и сравнительно небольшими, ошибками. Считают, что всякое титриметрическое определение включает в себя возможную ошибку титра рабочего раствора и возможную ошибку титрования анализируемого вещества. Первая зависит от точности взвешивания стандартного вещества и правильности измерения объема раствора. Вторая определяется точностью титрования, то есть правильностью установления точки эквивалентности с помощью индикатора: если капля рабочего раствора, прибавляемая к исследуемой жидкости, имеет слишком большой объем, то этим создается вероятность добавки не строго эквивалентного, а большего количества вещества.
Выполняя титриметрические определения, стремятся к тому, чтобы точность их достигала 0,1 %. Естественно, что для этого каждая отдельная операция анализа должна быть выполнена с не меньшей точностью.
Ошибки титриметрического анализа подразделяют на систематические и случайные. Обычно систематические ошибки очень невелики.
Пример. Пусть вблизи точки эквивалентности оставалось недотитрованным такое количество вещества, на которое необходимо израсходовать только 0,01 см3 рабочего раствора. Но объем прибавляемой из бюретки капли равен 0,06 см3, и добавление ее вызвало избыток рабочего раствора на 0,06 – 0,01 = 0,05 см3. Если при этом на все титрование было израсходовано 25,00 см3 рабочего раствора, то избыток в 0,05 см3 составляет 0,2 %. Очевидно, что в рассматриваемом случае точность окончательного результата анализа уже не может стать выше 0,2%. Поэтому при выполнении титриметрических определений стремятся, чтобы объем вытекающих капель был возможно меньшим.
Когда исследуемое вещество титруют в тех же условиях, в каких устанавливался титр рабочего раствора, ошибки, допущенные при этих операциях, могут оказаться приблизительно одинаковыми, но противоположными по знаку. В таком случае систематические ошибки взаимно компенсируют друг друга.
На результат анализа могут оказать влияние и случайные ошибки. Чтобы устранить их, титриметрическое определение повторяют несколько раз и берут среднее из них. Однако, вычисляя средний результат, допускают отклонение не более 0,3 %. Результаты определений, отличающиеся на большую величину, отбрасывают при вычислении среднего арифметического.
Пример. Если в четырех определениях нормальности раствора едкого натра были получены величины 0,1134; 0,1132; 0,1142; 0,1136, то число 0,1142 отбрасывают; оно отличается от наименьшего числа 0,1134 на 0,7%. Из остальных величин берут среднее арифметическое.
Нельзя удовлетворяться недостаточно близкими результатами титрования и не следует добиваться недостижимой сходимости результатов титрования.
Титрованные растворы должны быть свежими. Титр после хранения следует проверять. Титрованные растворы, на которые действует свет (например, раствор серебра), следует хранить в темных бутылях. Титр растворов марганцевокислого калия, а также веществ, способных изменяться при контакте с воздухом или стеклом, следует устанавливать не ранее, чем через 3…4 дня после приготовления. Титрованные растворы щелочей лучше хранить в бутылях, покрытых изнутри парафином и защищать их от действия диоксида углерода воздуха хлоркальциевой трубкой с натронной известью. Все бутыли с титрованными растворами должны иметь надпись с указанием вещества, нормальности, поправки, даты приготовления раствора и проверки титра.
Водные растворы следует готовить только на дистиллированной воде. Нельзя наливать сразу все нужное количество воды в колбу. Точный объем жидкости можно получить только при температуре, при которой была калибрована колба. Перед использованием раствора следует установить его концентрацию или поправку. Все растворы следует готовить только в хорошо вымытой посуде. Нельзя путать пробки от посуды, содержащей растворы разных веществ. Растворы щелочей следует готовить очень концентрированными, отстаивать, фильтровать, а затем разбавлять. Растворы, за исключением точных, после приготовления фильтруют.
