Практическая работа № 1.
Приёмы обращения с лабораторным оборудованием и
нагревательными приборами.
Цель работы: 1. Изучить правила техники безопасности при
работе в
химической лаборатории (кабинете).
2.
Познакомиться с устройством и основными приёмами
обращения с лабораторным оборудованием.
Оборудование: Штатив, спиртовка, пробирка, стакан с водой,
лабораторная
посуда.
Ход работы.
I. Правила
техники безопасности при работе в химической лаборатории (кабинете).
1. Категорически запрещается:
·
брать вещества руками.
Твёрдые вещества можно брать из баночек только сухой специальной ложкой,
насыпать твёрдые вещества и наливать жидкости нужно осторожно и только над
столом или специальным поддоном;
·
пробовать вещества на
вкус;
·
нюхать вещества из
горлышка склянок, т.к. вдыхание паров и газов может вызвать раздражение
дыхательных путей. Для ознакомления с запахом нужно ладонью руки сделать
движение от отверстия сосуда к носу (рис. 112);
·
при смешивании веществ в
пробирке зажимать отверстие пальцем;
·
смешивать вещества без
указания учителя.
2. Проводить опыты только с теми веществами,
которые указаны учителем.
3. Проводить опыты только с таким количеством
веществ, которые указаны в
инструкции.
4. Спиртовку зажигать только спичкой! НЕЛЬЗЯ
зажигать спиртовку зажигалкой,
горящей бумагой
или другой спиртовкой, т.к. может пролиться спирт и
возникнет пожар!
НЕЛЬЗЯ ни в коем случае держать голову близко к пламени
или наклоняться
над ним.
5. Тушить пламя спиртовки только колпачком!
6. При нагревании вещества в пробирке её сначала
необходимо целиком прогреть
над пламенем; отверстие
пробирки направлять в сторону от себя, и от соседей.
7. Соблюдать особую осторожность при работе с
едкими веществами –
кислотами и щелочами!
ПОМНИТЕ – при разбавлении кислоту медленно
наливают
тонкой струйкой в воду!!!
8. В случае ожога, пореза или попадания едкой и
горячей жидкости на кожу или
одежду следует немедленно
обратиться к учителю или лаборанту!
9. Не загромождать рабочее место посторонними
предметами, бережно
обращаться с лабораторным
оборудованием!
10. Закончив работу, привести рабочее место в
порядок!
II. Лабораторное оборудование.
1. Устройство
лабораторного штатива.
Задание: рассмотреть и нарисовать штатив, обозначить
его составные части.
|
|
1. 2. 3. 4. 5. |
2. Устройство
спиртовки.
Задание 1: рассмотреть и нарисовать спиртовку,
обозначить её составные
части.
|
|
1.Сосуд 2.Фитиль 3.Металлическая трубка с диском 4.Колпачок |
Задание 2: налить в пробирку 2 мл воды, закрепить
пробирку
в держателе, нагреть воду до кипячения.
3. Химическая
посуда.
Задание: рассмотреть и нарисовать образцы химической
посуды.
Практическая работа № 2.
Наблюдение за горящей свечой.
Цель работы: 1. Изучить строение пламени.
2. Изучить явления, происходящие при горении свечи. Оборудование: Свеча, предметное стекло, пробирки, лучина, резиновая
груша, 2 химических стакана разного объёма.
Ход работы.
Опыт 1. Физические явления при горении свечи:
Задание: Зажечь свечу. Что наблюдаете?
Наблюдение: таяние парафина. Это физический процесс – плавление.
Вывод:
Опыт 2. Обнаружение продуктов горения в пламени.
Задание 1: Возьмите тигельными щипцами предметное стекло,
внесите в зону темного конуса горящей свечи и подержите 3-5 с. Что наблюдаете?
Дайте объяснение.
Наблюдение: на
предметном стекле, внесённом в зону темного конуса пламени, образовалось чёрное
пятно – сажа.
Вывод:
Задание 2: Сухую пробирку закрепите в держателе, переверните
вверх дном и подержите над пламенем. Что наблюдаете? Дайте объяснение.
Наблюдение: сухая пробирка, находящаяся над пламенем запотела.
Вывод:
Задание 3: В ту же пробирку быстро прилить известковой воды. Что
наблюдаете? Дайте объяснение.
Наблюдение: в эту же пробирку быстро прилили известковой воды,
она помутнела.
Вывод:
Задание 4: Рассмотрите, какое строение имеет пламя. Поместите
лучину (спичку) в пламя спиртовки так, чтобы она проходила через все зоны. Что
наблюдаете? Дайте объяснение.
Опыт 3. Влияние воздуха на горение свечи.
Задание 1: Вставьте стеклянную трубку с оттянутым концом в
резиновую грушу. Сжимая её рукой, продуйте в пламя горящей свечи воздух. Что
наблюдаете? Дайте объяснение.
Наблюдение:
усиление яркости пламени при продувании грушей около пламени.
Вывод:
Задание 1: Зажгите две свечи и накройте их стаканами разного
объёма. Что наблюдаете? Дайте объяснение.
Наблюдение: горение свечи дольше под стаканом большего объёма.
Вывод:
Данные инструкции удобно применять при проведении практических работ по химии в 8 классе и не только по учебно-методическому комплексу О.С.Габриеляна, но и при проведении практических работ в других авторских комплексах. Удобство данних инструкции заключается в том, что при их использовании учащиеся учатся правильно оформлять практические работы, правильно делать выводы из работы. Пошаговая разработка опытов, позволяет учащимся сократить время для определения последовательности проведения практических опытов.
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Практическая работа №1»
Просмотр содержимого документа
«Практическая работа №2»
Просмотр содержимого документа
«Практическая работа №3»
Просмотр содержимого документа
«Практическая работа №4»
Просмотр содержимого документа
«Практическая работа №5»
Просмотр содержимого документа
«Практическая работа №6»
Просмотр содержимого документа
«Практическая работа №7»
ГРАФИК ВЫПОЛНЕНИЯ ПРАКТИЧЕСКОЙ ЧАСТИ
ПЕРЕЧЕНЬ ЛАБОРАТОРНЫХ РАБОТ
|
№ |
ТЕМА |
ДАТА |
|
1 |
Рассмотрение веществ с различными физическими свойствами. |
|
|
2 |
Разделение смесей. |
|
|
3 |
Рассмотрение коллекций металлов. |
|
|
4 |
Знакомство с образцами оксидов. |
|
|
5 |
Действие индикаторов на растворы щелочей. |
|
|
6 |
Действие индикаторов на растворы кислот. |
|
|
7 |
Разложение СиСО3, Си(ОН)2. |
|
|
8 |
Получение сульфида железа (II). |
|
|
9 |
Взаимодействие железа с раствором сульфата меди. |
|
|
10 |
Реакции обмена между растворами. |
|
|
11 |
Получение из пероксида водорода кислорода. |
|
|
12 |
Растворимость сахара в воде при разной температуре. |
|
|
13 |
Реакции обмена между электролитами, идущие до конца. |
|
|
14 |
Взаимодействие NaOH c H2SO4, c CO2, c CuSO4. Разложение Cu(OH)2. Взаимодействие Cu(OH)2 с H2SO4. |
|
|
15 |
Изучение свойств основных оксидов. |
|
|
16 |
Изучение свойств солей: а) взаимодействие CuSO4 с Fe; б) взаимодействие CuSO4 с NaOH; в) взаимодействие Na2SO4 с BaCl2; г) взаимодействие Na2CO3 с HCl. |
ПЕРЕЧЕНЬ ПРАКТИЧЕСКИХ РАБОТ
|
№ |
ТЕМА |
ДАТА |
|
1 |
ПТБ. Приемы обращения с лабораторным оборудованием. |
|
|
2 |
Способы разделения смесей. Очистка загрязненной поваренной соли. |
|
|
3 |
Приготовление раствора сахара и определение массовой доли сахара в растворе |
|
|
4 |
Условия течения химических реакций между растворами электролитов до конца |
|
|
5 |
Решение экспериментальных задач по теме «Основные классы неорганических соединений». |
ИНСТРУКЦИЯ ПО ОХРАНЕ ТРУДА ДЛЯ УЧАЩИХСЯ ПРИ РАБОТЕ В КАБИНЕТЕ ХИМИИ
ОБЩИЕ ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
- Соблюдение требований настоящей инструкции обязательно для учащихся, работающих в кабинете.
- Запишите на обложке тетради номер своего рабочего места в кабинете химии.
- Пребывание учащихся в помещении кабинета разрешается только а присутствии учителя химии; пребывание учащихся в лаборантской запрещается.
- Портфели, сумки и другие вещи следует убирать в ящики стола. Во время работы на столе должны находиться только: необходимое оборудование, тетрадь и письменные принадлежности.
- В ходе выполнения работы по одному варианту координируйте свои действия с действиями соседа по парте, разговаривая при этом шепотом.
- Перед началом ЛО, ПР учащиеся должны изучить правила пользования устройством для смыва капель жидкости с кожи и промывалки глаз (УПГ).
- Прежде чем приступить к выполнению ПР, следует подготовиться к ней, уяснить цели и задачи, прочитав инструкцию по ее выполнению и внимательно выслушав объяснение учителя.
- Уборку рабочих мест по окончании работы следует проводить в соответствии с инструкцией к работе и указаниями учителя.
- После окончания работы сдать рабочее место дежурному по классу. По окончании ПР учащиеся должны тщательно вымыть руки с мылом.
- При получении травмы, а также при плохом самочувствии учащиеся должны немедленно сообщить об этом учителю.
- При необходимости ученик должен уметь пользоваться содержимым аптечки и согласно инструкции уметь оказать первую помощь при порезах и ожогах.
- При возникновении в кабинете во время занятий аварийных ситуаций (пожар, появление сильных посторонних запахов) не допускать паники и подчиняться только указаниям учителя.
ТРЕБОВАНИЯ БЕЗОПАСНОСТИ ВО ВРЕМЯ РАБОТЫ
В КАБИНЕТЕ ХИМИИ
ЗАПРЕЩАЕТСЯ:
- Есть, пить в химическом кабинете, пробовать вещества на вкус;
- Брать вещества руками;
- Оставлять неубранными рассыпанные или разлитые реактивы;
- Выливать или высыпать отработанные реактивы в раковину;
- Выливать или высыпать остатки реактивов в склянки и банки, из которых они были взяты;
- Набирать ртом при помощи пипетки ядовитые и едкие жидкости;
- Набирать одной и той же ложечкой или пипеткой различные вещества;
- Менять пробки и пипетки от различных банок или склянок;
- Оставлять открытыми склянки с жидкостями и банки с сухими веществами;
- Работать с легковоспламеняющимися веществами вблизи огня;
- Переходить на другие рабочие места без разрешения учителя;
- Перебрасывать друг другу какие-либо предметы;
- Бесцельно смешивать растворы или испытывать вещества по собственному усмотрению, проводить самостоятельно любые опыты, не предусмотренные данной работой;
- Уносить с собой что бы то ни было из предметов и веществ, предназначенных для проведения опытов;
- Зажигать спиртовку без надобности;
- Оставлять пробирки и другую химическую посуду грязной.
КРАТКАЯ ИНСТРУКЦИИ ПО ОКАЗАНИЮ МЕР ПЕРВОЙ ПОМОЩИ
ПРИ РАЗЛИЧНОГО РОДА ОТРАВЛЕНИЯХ ИЛИ ПОРАЖЕНИЯХ ОРГАНИЗМА
|
Поражения |
Первая помощь |
|
При порезах стеклом |
Обработать рану 3%-ным водным раствором пероксида водорода для остановки кровотечения. Затем продезинфицировать водным раствором KMnO4 или спиртом, смазать йодом и наложить повязку. После оказания первой помощи направить к врачу. |
|
При ожогах: 1. термическом (огнем, горячим паром, горячим предметом) А) первой степени (краснота) Б) второй степени (пузыри) В) третьей степени (разрушение тканей) — — — — — — — — — — — — — — — — — — — — 2. кислотном (серной, азотной, фосфорной), хлором или бромом — — — — — — — — — — — — — — — — — — — — — 3. щелочном |
Для снятия болевых ощущений смазать место ожога глицерином. Наложить повязку с ватой, смоченной этиловым спиртом. Обработать аналогично ожогу первой степени, а затем 3 – 5%-ным водным раствором KMnO4 или 5%-ным водным раствором танина. Наложить стерильную повязку. Пострадавшего направить к врачу. Покрыть рану стерильной повязкой и направить пострадавшего к врачу. — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — Промыть пораженный участок кожи большим количеством воды (УПГ), затем 5%-ным водным раствором NaHCO3 (соды). Наложить повязку с ватой, смоченной риванолом или фурацилином. Для обработки глаз после промывания струей воды (УПГ) использовать 3%-ный водный раствор NaHCO3 (соды). — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — Участок кожи обильно промыть водой (УПГ). Глаза промыть струей воды (УПГ). Затем глаза и кожу обработать 2%-ным водным раствором борной кислоты Н3ВО3. |
|
При отравлениях: А) кислотами — — — — — — — — — — — — — — — — — — — — Б) щелочами — — — — — — — — — — — — — — — — — — — — — В) газами |
Вызвать рвоту (например, выпив 1%-ный водный раствор CuSO4), сделать промывание желудка. Принять внутрь 4 – 6 таблеток или одну столовую ложку активированного угля или 250 гр крахмального клейстера. Пить кашицу из оксида магния. — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — Первая помощь как при отравлении кислотами. Затем пить 1%-ный водный раствор лимонной или уксусной кислоты. — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — Обеспечить доступ чистого воздуха и покой. В тяжелых случаях — кислород. |
|
При поражениях электрическим током |
Обеспечить доступ свежего воздуха. Дать понюхать вату, смоченную 10%-ным водным раствором аммиака. При наличии электрического удара (отсутствие дыхания, не бьется сердце) – искусственное дыхание, резиновая грелка. |
ПРАКТИЧЕСКАЯ РАБОТА №1
ПРИЕМЫ ОБРАЩЕНИЯ С НАГРЕВАТЕЛЬНЫМИ ПРИБОРАМИ.
Цель работы:
- познакомиться с устройством нагревательных приборов, отработать приемы и правила обращения с ними;
- изучить строение пламени спиртовки, определить практически влияние воздуха на горние свечи.
Техника безопасности:
Запрещается передавать зажженную спиртовку и зажигать одну спиртовку от другой, т.к. при наклонении может пролиться спирт вызвать пожар.
Гасить спиртовку, только накрыв пламя колпачком или крышкой.
Инструкция к работе
1. Рассмотрите спиртовку. Найдите ее составные части: резервуар, колпачок, трубка с диском, фитиль.
2. Проверьте:
— правильность заполнения спиртовки (не менее чем на 2∕3 ее объема) спиртом;
— состояние фитиля в трубке: он должен быть ровно подрезан, его длина 1,5 см над диском;
— положение фитиля в трубке: он должен неплотно прилегать, но и не выпадать из трубки;
— положение диска с трубкой: он должен плотно прикрывать отверстие резервуара спиртовки.
3. Отработайте приемы зажигания спиртовки спичкой или горящей лучинкой и ее тушения (колпачком или крышкой).
4. Рассмотрите пламя. Оно неоднородно: выделите три зоны.
5. Исследуйте каждую зону пламени, вносите в нее на короткое время лучину (или спичку). Определите цвет пламени (менее яркое, яркое, темное) и по характеру обугливания лучины отметьте характеристику зон по температуре (самая горячая, менее горячая, холодная).
6. Исследуйте внутреннюю часть пламени. Для этого возьмите тигельными щипцами стеклянную трубку (держите ее под углом) и внесите одним концом во внутреннюю часть пламени, а к другому концу поднесите горящую лучину. Что при этом наблюдается?
7. Исследуйте среднюю часть пламени. Для этого холодный предмет (например, фарфоровую чашку) внесите на 2 – 3 сек в самую яркую часть пламени. Что вы обнаружили?
8. Определите продукты горения, которые образуются во внешней части пламени. Для этого сухую пробирку закрепите в держателе, переверните вверх дном и подержите над пламенем до запотевания. Объясните наблюдаемое явление. В ту же пробирку быстро прилейте 2 – 3 мл известковой воды и взболтайте ее. Что вы обнаружили?
9. Пользуясь спиртовкой, нагрейте в пробирке небольшой объем воды:
— налейте в пробирку 1 мл воды (примерно 20 капель);
— поместите пробирку в пробирочный зажим (зажимная часть его должна находиться у ранта (отверстия) пробирки);
— внесите пробирку в самую горячую часть пламени и нагрейте ее по всей длине двумя – тремя движениями в пламени спиртовки;
— не вынимая из пламени, нагрейте то место, где находится вода;
— направляйте отверстие нагреваемой пробирки в сторону от себя и соседа по парте, избегая выбрасывания жидкости;
— чтобы вода не выплеснулась из пробирки, проводите все время круговые движения, но не прикасайтесь ее дном к фитилю, т.к. пробирка может лопнуть от соприкосновения с относительно холодным и мокрым фитилем;
— не наклоняйтесь над нагревательным сосудом (пробиркой);
— когда закипит вода, прекратите нагревание.
Спиртовку закройте колпачком. Нагретую пробирку поставьте в штатив для пробирок.
10. Приведите рабочее место в порядок.
11. Оформите отчет о проделанной работе. При оформлении отчета используйте материал учебника: стр. 176 – 177, рис. 114.
Отчет:
Оборудование: _____________________________________________________________________
Реактивы: _________________________________________________________________________
|
Действия (выполняемые операции, рисунки с поясняющими надпи-сями) |
Что наблюдал? Уравнения реакций |
Выводы |
|
1. Изучение устройства спиртовки (рисунок) 2. Отрабатывание приемов обращения со спиртовкой. |
Составные части спиртовки: |
При хранении спиртовка должна быть _____________ , чтобы ____. Диск с трубкой должен плотно прикрывать отверстие резервуара спиртовки, иначе во время работы может _____________________ . Спиртовка зажигается только ___. Пламя спиртовки гасится _______. |
|
3. Изучение строение пламени (рисунок). |
Пламя состоит из ______ зон, каждая из которых имеет ______________, цвет: _____. |
Наиболее высокая температура пламени в ______ зоне, поэтому при нагревании предметы необходимо помещать в ______. |
|
4. Исследование составных частей пламени: а). во внутреннюю часть пламени тигельными щип-цами вносили стеклянную трубочку одним концом, а к другому концу подносили горящую лучинку; — — — — — — — — — — — — — — — — — — — — б). в среднюю часть пламени на короткое время вносили фарфоровую чашку; — — — — — — — — — — — — — — — — — — — — в) Для определения состава внешней части пламени вносили в нее перевернутую вверх дном пробирку. Затем в пробирку прилили известковую воду. |
Наблюдали: ___________________________ — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — Фарфоровая чашка ___________________ — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — — Стенки пробирки ____________________ . Известковая вода ____________________ . |
Внутренний конус образован ____________________________ — — — — — — — — — — — — — — — — — — — — — — — — — В среднем конусе содержится _______________________, который образуется при ________. — — — — — — — — — — — — — — — — — — — — — — — — — Внешний конус пламени содержит конечные продукты сгорания: ___________________ . |
|
5. Нагревание на открытом пламени пробирки с водой (пробирка укреплена наклонно). (Рисунок) |
Вода в пробирке ______________________ . |
Пробирка в лапке пробиркодер-жателя закрепляется так, чтобы ее можно было повернуть, не прилагая усилий, т.к. при нагревании тела _____________ . |
Приведите рабочее место в порядок.
ПРАКТИЧЕСКАЯ РАБОТА №2
СПОСОБЫ РАЗДЕЛЕНИЯ СМЕСЕЙ. ОЧИСТКА ПОВАРЕННОЙ СОЛИ.
Цель работы:
1. ознакомиться со способами разделения смесей;
2. освоить простейшие способы очистки веществ;
3. отработать навыки работы с химическим оборудованием.
Инструкция к работе
Задание 1.
Рассмотрите выданную смесь поваренной соли и песка. Какие физические свойства характерны для поваренной соли и песка? Заполните таблицу:
|
Поваренная соль |
Песок |
|
|
1. Агрегатное состояние |
||
|
2. Цвет |
||
|
3. Запах |
||
|
4. Растворимость в воде |
Задание 2. Растворение загрязненной поваренной соли в воде
- В химический стакан налейте 7 – 8 мл воды.
- Добавьте при помешивании загрязненную поваренную соль. Раствор помешивайте осторожно с помощью стеклянной палочки.
- Рассмотрите полученный раствор. Опишите, что вы наблюдаете (цвет, частицы в стакане и т. д.)
Задание 3. Очистка неоднородного раствора соли фильтрованием.
- Пользуясь указаниями учителя, приготовьте фильтр.
- Фильтр поместите в воронку.
- Налейте на фильтровальную бумагу, вставленную в воронку, немного воды , смочите весь фильтр.
- Воронку с фильтром вставьте в кольцо штатива.
- Подставьте к концу воронки чистый стакан.
- По стеклянной палочке наливайте загрязненный раствор поваренной соли.
- Опишите, что осталось на фильтре.
- Каков внешний вид фильтрата?
- В состав фильтрата входят: ….?
- Какие свойства поваренной соли и песка лежат в основе проведенного способа разделения смеси?
Задание 4.
Сделайте рисунок прибора для фильтрования, обозначьте его основные детали:
- штатив;
- воронка;
- фильтр;
- стеклянная палочка;
- химический стакан;
- раствор загрязненной поваренной соли;
- фильтрат;
- кольцо.
Задание 5. Выпаривание очищенного раствора соли.
- В фарфоровую чашку налить 1 мл фильтрата.
- Установите фарфоровую чашку с фильтратом на кольцо штатива.
- Зажгите спиртовку и проведите выпаривание фильтрата.
- Опишите внешний вид полученной чистой соли.
- Ответьте на вопрос: Какие свойства соли и воды лежат в основе проведенного способа разделения смеси?
Приведите рабочее место в порядок.
Оформите отчет о проделанной работе. При оформлении отчета используйте материал учебника: §25, рис. 82, 83.
Отчет:
Оборудование:______________________________________________________________________
Реактивы: _________________________________________________________________________
|
Действия (выполняемые операции, рисунки с поясняющими надпи-сями) |
Что наблюдал? Уравнения реакций |
Выводы |
|
Растворение загряз-ненной поваренной соли в воде (рисунок) |
Опишите, что вы наблюдаете: цвет раствора, частицы в стакане ___________________________________ |
В воде находятся______________ ______________________________ |
|
Очистка неоднородного раствора соли фильт-рованием. (рисунок) |
|
|
|
Выпаривание очищен-ного раствора соли. (рисунок) |
Какие свойства соли и воды лежат в основе проведенного способа разделения смеси? |
ПРАКТИЧЕСКАЯ РАБОТА №3
ПРИГОТОВЛЕНИЕ РАСТВОРА САХАРА И ОПРЕДЕЛЕНИЕ МАССОВОЙ ДОЛИ САХАРА В РАСТВОРЕ
Цель работы:
- закрепить важнейшие химические понятия: относительная молекулярная и молярная массы, количество вещества, моль, постоянная Авогадро, массовая доля растворенного вещества;
- научиться выполнять такие лабораторные операции, как взвешивание, отбор проб твердых и жидких веществ, приготовление растворов;
- практически закрепить химические расчеты с использованием указанных выше физико-химических характеристик.
Инструкция к работе
1. Отмерьте мерным цилиндром 50 мл воды и влейте ее в коническую колбу емкостью 100 мл.
2. Рассчитайте массу сахара и приготовьте раствор сахара. Для этого:
- соберите весы;
- поместите на левую чашку весов кружок фильтровальной бумаги и уравновесьте весы, размещая разновесы на правой чашке.
- на кружок фильтровальной бумаги поместите чайную ложку сахарного песка и взвесьте;
- взвешенный сахар перенесите в колбу с водой и перемешайте стеклянной палочкой до полного растворения.
3. Рассчитайте массовую долю сахара в полученном вами растворе:
ω = mсахара : mраствора; mраствора = mсахара + mводы;
mводы = V воды · ρ воды; ρ воды = 1гр∕мл
4. Рассчитайте число молекул сахара в полученном вами растворе:
Nмолекул сахара = NA · nсахара; nсахара = mсахара : Мсахара
Сахар на 99,9% состоит из сахарозы, имеющей формулу С12Н22О11.
Сделайте расчеты молекулярной относительной и молярной массы сахара.
5.* Рассчитайте число молекул в одном глотке раствора сахара:
Nмолекул сахара в одном глотке = Nмолекул сахара в растворе : 15, где 15 – число глотков.
6. Приведите свое рабочее место в порядок.
7. Составьте отчет о проделанной работе.
ОТЧЕТ:
Оборудование: ______________________________________________________________________
Реактивы: __________________________________________________________________________
|
Действия (выполняемые операции, рисунки с поясняющими надпи-сями) |
Расчетная часть |
Выводы |
|
1. Отмерьте мерным цилиндром 50 мл воды и влейте ее в коническую колбу емкостью 100 мл (рисунок) |
V воды = 50 мл |
Уровень жидкости прозрачных растворов устанавливается по __________________________ . |
|
2. Взвесить __________на лабораторных весах. (рисунок), указать, на какую чашу весов ставят разновесы, а на какую – вещество. |
mсахара = ______гр |
Для приготовления раствора нужно: ____________________. |
|
3. Взвешенный сахар массой ____гр растворить в 50 мл воды. |
mраствора = mсахара + mводы; mраствора = _______гр |
Полученный раствор представляет собой ___________________________ (Указать: однородную или неоднородную смесь) |
|
4. Выполнить расчеты: Дано: V воды = 50 мл mсахара = ____гр mраствора = ____гр Найти: ωсахара % |
ωсахара % = __________ Nмолекул сахара = __________ |
ПРАКТИЧЕСКАЯ РАБОТА №4
УСЛОВИЯ ТЕЧЕНИЯ ХИМИЧЕСКИХ РЕАКЦИЙ МЕЖДУ РАСТВОРАМИ ЭЛЕКТРОЛИТОВ ДО КОНЦА
Цель работы:
- совершенствовать навыки проведения химических экспериментов;
- практическим путем подтвердить условия проведения реакций ионного обмена.
Инструкция к работе
Задание 1 Реакции ионного обмена, сопровождающиеся образованием осадка.
Возьмите две пробирки. Налейте в каждую пробирку по 2 – 3 мл раствора: в №1 – хлорида натрия, в №2 – фосфата натрия. Затем в каждую пробирку добавьте несколько капель раствора нитрата серебра. Отметьте цвет полученных осадков.
В пробирке №1 осадок _____________________ цвета.
В пробирке №2 осадок _____________________ цвета.
Задание 2 Реакции ионного обмена, сопровождающиеся выделением газообразного вещества.
Возьмите две пробирки. В №1 налейте 2 – 3 мл раствора карбоната натрия, в №2 – столько же сульфата калия. В каждую из пробирок добавьте несколько капель раствора соляной кислоты. Что наблюдаете?
————————————————————————————————————————————————————————————————————————————————————
Задание 3 Реакции ионного обмена, сопровождающиеся образованием малодиссоциирующего вещества.
- В пробирку №1 налейте 2 – 3 мл раствора гидроксида натрия и добавьте 1 – 2 капли раствора ф – ф. как изменилась окраска раствора индикатора?
Раствор индикатора был _________ цвета, а стал __________ цвета.
- Прилейте раствор соляной кислоты до полного обесцвечивания. Почему окраска индикатора исчезла?
—————————————————————————————————————————
- В пробирку №2 налейте 4 – 5 мл раствора сульфата меди (II). Каков цвет раствора?
Раствор сульфата меди (II) имеет ___________ окраску.
- Добавьте к нему 2 – 3 мл раствора гидроксида натрия. Что наблюдаете?
——————————————————————————————————————————-
- Прилейте избыток раствора соляной кислоты. Что наблюдаете?
——————————————————————————————————————————
Задание 4. Результаты экспериментальной части работы запишите в таблицу отчета. При составлении отчета воспользуйтесь §§ 37, 38, 39,41.
ОТЧЕТ:
Оборудование: _____________________________________________________________________
Реактивы: ________________________________________________________________________
|
Действия (выполняемые операции, рисунки с поясняющими надпи-сями) |
Что делали? |
Что наблюдали? |
Выводы Ответы на контрольные вопросы |
|
Задание 1. Реакции ионного обмена, сопровождающиеся обра-зованием осадка. Пробирки: №1 – хлорида натрия, №2 – фосфата натрия |
№1 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
В пробирке №1 осадок _ _ _ _ _ цвета |
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|||
|
№2 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
В пробирке №2 осадок _ _ _ _ _ цвета. |
|
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|||
|
Задание 2. Реакции ионного обмена, сопровождающиеся выде-лением газообразного вещества. Пробирки: №1 — раствор карбоната натрия, №2 – сульфата калия |
№1 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|||
|
№2 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|||
|
Задание 3. Реакции ионного обмена, сопровождающиеся обра-зованием малодиссоци-ирующего вещества. Пробирки: №1 — раствор гидроксида натрия №2 — раствора сульфата меди (II). |
№1 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
Раствор индикатора был _ _ _ цвета, а стал _ _ _ цвета |
Почему окраска индии-катора исчезла после добавления раствора соляной кислоты? |
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|||
|
№2 _ _ _ _ _ _ _ _ _ _ _ _ _ 1). Добавьте раствор гид-роксида натрия. 2). Прилейте избыток раствора соляной кислоты. |
Раствор сульфата меди (II) имеет _ _ _ _ _ _ _ _ окраску. Что наблюдаете после добавления раствора гидроксида натрия? Что наблюдаете? |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ __ _ _ _ _ _ _ _ _ |
|
|
1). Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|||
|
2). Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
Приведите свое рабочее место в порядок.
Задание 5*. Обсудите возможность практического осуществления химических реакций между растворами следующих веществ:
- гидроксида калия и хлорида бария;
- сульфида натрия и соляной кислоты;
- силиката калия и азотной кислоты;
- гидроксида бария и серной кислоты.
Составьте уравнения (в молекулярном, полном и сокращенном ионном виде) для возможных реакций.
ПРАКТИЧЕСКАЯ РАБОТА №5
РЕШЕНИЕ ЭКСПЕРИМЕНТАЛЬНЫХ ЗАДАЧ ПО ТЕМЕ:
«ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ»
Цель работы:
- повторить свойства оксидов, оснований, кислот, солей и применить эти знания при экспериментальном решении задач;
- научиться распознавать вещества, помещенные в склянки без этикеток;
- научиться оформлять экспериментальное решении задач этого типа в отчете о практической работе.
Инструкция к работе:
1. Особенностью экспериментального решения задач является то, что для опыта берут определенную порцию вещества — «пробу». При распознавании веществ, при проведении нескольких разных опытов с одним веществом или при решении задачи разными способами берут несколько проб. Чтобы не перепутать пробирки с растворами, ставьте их друг за другом в штатив для пробирок.
2. Каждую экспериментальную задачу можно решить несколькими способами – выберите из них самый рациональный, т.е. тот, в котором нужный результат достигается при выполнении меньшего числа операций.
3. Составьте план решения задач.
4. Проверьте наличие на рабочем месте необходимого оборудования, реактивов.
5. Решите задачи одного из предложенных учителем вариантов.
6. Вымойте посуду и приведите рабочее место в порядок.
7. Оформите отчет о проделанной работе.
Вариант 1.
Реактивы: вода, смесь железа и сахара, растворы хлорида бария, хлорида железа (III), гидроксида натрия, в склянке без этикетки раствор сульфата натрия, в пробирках №№1, 2, 3 растворы сульфата натрия, карбоната натрия, фосфата натрия.
Вариант 2.
Реактивы: вода, смесь железа и соли, растворы соляной кислоты, серной кислоты, нитрата серебра, хлорида бария, сульфата меди (II), гидроксида натрия, в склянке без этикетки раствор сульфата натрия, в пробирках №№1, 2, 3 растворы хлорида калия, сульфата калия, фосфата калия.
Задание 1.
Исходя из свойств веществ, разделите вам смесь. Ответ изобразите в виде рисунка с обозначениями.
Задание 2.
В склянке без этикетки находится бесцветный раствор. Предполагается, что это:
Вариант 1: раствор хлорида калия
Вариант 2: раствор сульфата натрия.
Проведите опыт, подтверждающий данное предположение. Результат занесите в таблицу отчета. Уравнения запишите в молекулярной и ионной формах.
Задание 3.
В пробирках №№1, 2, 3 находятся растворы следующих веществ:
Вариант 1: растворы сульфата натрия, карбоната натрия, фосфата натрия.
Вариант 2: растворы хлорида калия, сульфата калия, фосфата калия.
Опытным путем докажите, в какой склянке находится каждое из веществ. Результаты внесите в отчет.
Задание 4*. Экспериментальным путем осуществите превращения:
Вариант 1: хлорид железа (III) → гидроксид железа (III) → вода.
Вариант 2: серная кислота → сульфат меди → гидроксид меди.
Составьте план проведения эксперимента и запишите уравнения химических реакций в молекулярном, ионном видах.
Приведите рабочее место в порядок.
ОТЧЕТ:
Оборудование: _____________________________________________________________________
Реактивы: ________________________________________________________________________
|
Действия (выполняемые операции, рисунки с поясняющими надпи-сями) |
Что делали? |
Что наблюдали? |
Выводы Ответы на контрольные вопросы |
|
|
Задание 1. Разделение смеси. (рисунок) |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ __ _ |
|
|
Задание 2. Распознавание вещества. (Качественная реакция на анион.) |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||||
|
Задание 3. Распознавание веществ в пробирках №№ 1, 2, 3 (Качественная реакция на анион.) |
№1: _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||||
|
№2: _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||||
|
№3: _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||||
|
Задание 4*. Экспериментальным пу-тем осуществите превра-щения |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
|
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||||
|
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
||
|
Уравнение реакции (в молекулярной и ионной формах): _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ |
Практическая работа № 1
по теме: «Правила техники безопасности при работе в химическом кабинете. Приемы обращения с лабораторным оборудованием и нагревательными приборами»
Инструктаж по технике безопасности.
Цель работы: Познакомиться с устройством и основными приемами обращения с лабораторным оборудованием.
Оборудование: Штатив, спиртовка, лабораторная посуда.
Ход работы
1. Устройство штатива (нарисовать штатив, обозначить его составные части)
|
2.Устройство спиртовки (нарисовать спиртовку, обозначить её составные части)
|
1.Сосуд 2.Фитиль 3.Металлическая трубка с диском 4.Колпачёк |
1.Снять колпачок 2.Прроверить плотно ли прилегает диск к отверстию сосуда 3. Зажечь спиртовку горящей спичкой (НЕЛЬЗЯ ЗАЖИГАТЬ СПИРТОВКУ ОТ ДРУГОЙ ГОРЯЩЕЙ СПИРТОВКИ!) 4. Погасить спиртовку накрыв пламя колпачком. |
3.Посуда (нарисовать пробирки, колбы, химический стакан)
4.Фильтрование
1. приготовить фильтровальную бумагу;
2. смочить фильтровальную бумагу;
3. вложить в воронку;
4. жидкость наливают, по стеклянной палочке, направляя её на стенку воронки;
5. фильтрат, стекает по стенке стакана, а не в центр, чтобы не выплёскивался.
Найти в тексте определения фильтрата, осадка и процесса фильтрования.
Практическая работа №2
по теме: «Наблюдения за изменениями, происходящими с горящей свечой, и их описание»
Цель: наблюдать физические и химические явления при горении свечи.
Оборудование: предметное стекло, свеча, спички, сухая пробирка, держатель.
Инструкция по технике безопасности:
-
Стекло – хрупкий материал, имеющий малое сопротивление при ударе и незначительную прочность при изгибе. Категорически запрещается использовать посуду, имеющую трещины и отбитые края.
-
Пробирку закрепляют в держателе так, чтобы от горлышка пробирки до держателя было расстояние 1 – 1, 5 см.
-
Предметное стекло вначале прогревают полностью, а затем вносят в зону тёмного конуса горящей свечи.
Первая помощь при ожогах:
Ожог первой степени обрабатывают этиловым спиртом, затем, для снятия болевых ощущений, глицерином и накладывают сухую стерильную повязку. Во всех остальных случаях накладывают стерильную повязку после охлаждения места ожога и обращаются в медпункт.
Первая помощь при порезах:
а) в первую очередь, необходимо остановить кровотечение (давящая повязка, пережатие сосуда);
б) если рана загрязнена, грязь удаляют только вокруг неё, но ни в коем случае – из глубинных слоёв раны. Кожу вокруг раны обеззараживают йодной настойкой или раствором бриллиантовой зелени;
в) после обработки рану закрывают стерильной салфеткой так, чтобы перекрыть края раны, и плотно прибинтовывают обычным бинтом;
г) после получения первой помощи обратиться в медпункт.
Опыт №1. Физические явления при горении свечи.
Зажгите свечу. Вы увидите, как начинает таять парафин около фитиля, образуя круглую лужицу. Какой процесс здесь имеет место?
Опыт №2. Обнаружение продуктов горения в пламени.
Возьмите предметное стекло, закрепите в держателе (т/б), внесите в зону тёмного конуса горящей свечи и подержите 3 – 5 с. Быстро поднимите стекло, посмотрите на нижнюю плоскость. Объясните, что там появилось.
Сухую пробирку закрепите в держателе (т/б), переверните вверх дном и держите над пламенем до запотевания. Объясните наблюдаемое явление.
Практическая работа № 3
по теме: «Анализ почвы и воды»
Цель: определить состав почвы, научиться фильтровать и выпаривать жидкость.
Оборудование: две пробирки, воронка, бумажный фильтр, стеклянная палочка, предметное стекло, спиртовка, стеклянный цилиндр с водой, пробка, универсальная индикаторная бумага.
Инструкция по технике безопасности:
-
Если зажечь спиртовку сразу же после снятия колпачка, загорается плёнка спирта на горлышке спиртовки как раз на том месте, где колпачок прилегает к горлышку. Пламя проникает под диск с трубкой, и пары спирта внутри резервуара загораются. Может произойти взрыв и выброс диска вместе с фитилём. Чтобы избежать этого, приподнимите на несколько секунд диск с фитилём для удаления паров .Если случится воспламенение паров, быстро отставьте в сторону предметы (тетрадь для практических работ) и позовите учителя.
-
Зажжённую спиртовку нельзя переносить с места на место, нельзя также зажигать одну спиртовку непосредственно от другой. Для зажигания спиртовки пользуйтесь спичками.
-
Гасить спиртовку можно только одним способом – накрыть пламя фитиля колпачком. Колпачок должен находиться всегда под рукой.
-
Предметное стекло закрепляется в держателе у одного из его краёв аккуратно. При этом учитывается, что стекло – хрупкий материал и может треснуть, если на него сильно надавить.
-
В процессе выпаривания воды из почвенной вытяжки вначале прогревается всё предметное стекло, а затем капля жидкости на нём.
Первая помощь при порезах:
а) в первую очередь, необходимо остановить кровотечение (давящая повязка, пережатие сосуда);
б) если рана загрязнена, грязь удаляют только вокруг неё, но ни в коем случае – из глубинных слоёв раны. Кожу вокруг раны обеззараживают йодной настойкой или раствором бриллиантовой зелени;
в) после обработки рану закрывают стерильной салфеткой так, чтобы перекрыть края раны, и плотно прибинтовывают обычным бинтом;
г) после получения первой помощи обратиться в медпункт.
Первая помощь при ожогах:
Ожог первой степени обрабатывают этиловым спиртом, затем, для снятия болевых ощущений, глицерином и накладывают сухую стерильную повязку. Во всех остальных случаях накладывают стерильную повязку после охлаждения места ожога и обращаются в медпункт.
Опыт №1. Механический анализ почвы.
В пробирку помещена почва. Прилейте к ней воду, объём которой должен быть в 3 раза больше объёма почвы. Закройте пробирку пробкой и тщательно встряхивайте 1 – 2 минуты. Наблюдайте за осадком частиц почвы и структурой осадков. Опишите и объясните свои наблюдения.
Опыт №2. Получение почвенного раствора и опыты с ним.
Приготовьте бумажный фильтр, вставьте его в чистую пробирку и профильтруйте полученную в первом опыте смесь почвы и воды. Перед фильтрованием смесь не следует встряхивать. Почва останется на фильтре, а собранный в пробирке фильтрат представляет собой почвенную вытяжку( почвенный раствор).
Несколько капель этого раствора с помощью стеклянной палочки поместите на предметное стекло и подержите его над пламенем спиртовки (т/б) до выпаривания воды. Что наблюдаете? Объясните.
Возьмите универсальную индикаторную бумагу, нанесите на неё стеклянной палочкой почвенный раствор. Сделайте вывод по результатам своих наблюдений.
Практическая работа № 4
по теме: «Приготовление раствора сахара и определение массовой доли его в растворе»
Инструктаж по технике безопасности
Цель: научиться взвешивать на лабораторных весах, определять объем жидкости с помощью мерного цилиндра, приготовлять раствор с определенной массовой долей вещества.
Оборудование и реактивы: химический стакан, палочка для перемешивания, мерный цилиндр, лабораторные весы, разновесы; сахар, вода.
Порядок выполнения работы
-
Рассчитайте массу сахара и массу воды, необходимые для приготовления необходимого вам раствора используя формул:
m(вещества) = m(раствора) · ω(вещества)
m(H2O) = m(раствора) — m(вещества)
Расчеты приведите в отчете о практической работе.
-
Определите объем воды, соответствующий вычисленной массе, используя формулу: V = m · ρ. Помните, что для воды ρ = 1 г/мл.
Расчет приведите в отчете о практической работе. -
С помощью мерного цилиндра отмерьте вычисленный объем воды. Перелейте воду в химический стакан.
-
На лабораторных весах взвесьте вычисленную массу сахара. Всыпьте сахар стакан с водой.
-
Перемешайте содержимое химического стакана до полного растворения сахара.
-
Сделайте вывод о том, что необходимо для приготовления раствора с определенной массовой долей растворенного вещества.
Практическая работа № 5
по теме: «Признаки химических реакций»
Цель: рассмотреть примеры химических реакций и выявить их признаки.
Оборудование: пробирки, медная проволока, спиртовка, оксид меди (II), раствор серной кислоты, мрамор, раствор соляной кислоты, растворы хлорида железа (III) и роданида калия, растворы сульфата натрия и хлорида бария.
Инструкция по технике безопасности:
-
Если зажечь спиртовку сразу же после снятия колпачка, загорается плёнка спирта на горлышке спиртовки как раз на том месте, где колпачок прилегает к горлышку. Пламя проникает под диск с трубкой, и пары спирта внутри резервуара загораются. Может произойти взрыв и выброс диска вместе с фитилём. Чтобы избежать этого, приподнимите на несколько секунд диск с фитилём для удаления паров .Если случится воспламенение паров, быстро отставьте в сторону предметы (тетрадь для практических работ) и позовите учителя.
-
Зажжённую спиртовку нельзя переносить с места на место, нельзя также зажигать одну спиртовку непосредственно от другой. Для зажигания спиртовки пользуйтесь спичками.
-
Гасить спиртовку можно только одним способом – накрыть пламя фитиля колпачком. Колпачок должен находиться всегда под рукой.
-
Кислоты – едкие вещества. Разрушают и раздражают кожу, слизистые оболочки.
-
Наливать кислоту надо так, чтобы при наклоне склянки этикетка, во избежание её порчи, оказывалась сверху.
-
Соединения меди в виде пыли при попадании на кожу, особенно в местах микротравм, могут вызвать раздражения, привести к аллергии в лёгкой форме.
-
Работать с соединениями бария нужно так, чтобы не допустить попадания их в рот, так как они токсичны. Для получения тяжёлого отравления достаточно дозы массой менее 0,5г. После завершения работы тщательно помыть руки с мылом под проточной водой.
Первая помощь при порезах:
а) в первую очередь, необходимо остановить кровотечение (давящая повязка, пережатие сосуда);
б) если рана загрязнена, грязь удаляют только вокруг неё, но ни в коем случае – из глубинных слоёв раны. Кожу вокруг раны обеззараживают йодной настойкой или раствором бриллиантовой зелени;
в) после обработки рану закрывают стерильной салфеткой так, чтобы перекрыть края раны, и плотно прибинтовывают обычным бинтом;
г) после получения первой помощи обратиться в медпункт.
Первая помощь при ожогах:
Ожог первой степени обрабатывают этиловым спиртом, затем, для снятия болевых ощущений, глицерином и накладывают сухую стерильную повязку. Во всех остальных случаях накладывают стерильную повязку после охлаждения места ожога и обращаются в медпункт.
Первая помощь при попадании кислоты на кожу рук:
Попавшие на кожу капли кислоты стряхните и тщательно смойте большим количеством воды, а затем обработайте поражённую поверхность 2% раствором питьевой соды.
Первая помощь при отравлении солями бария:
Промыть желудок 1% раствором сульфата натрия или сульфата магния.
Опыт №1 Прокаливание медной проволоки.
Зажгите спиртовку. Возьмите тигельными щипцами медную поволоку и внесите ее в пламя. Через некоторое время уберите проволоку из пламени. Что наблюдаете?
Составьте отчет, заполнив таблицу.
Опыт №2 Взаимодействие карбоната натрия с соляной кислотой.
Положите в небольшой химический стакан немного карбоната натрия. Налейте в химический стакан столько соляной кислоты, чтобы карбонат натрия покрылся ею. Что наблюдаете?
Зажгите лучину и внесите ее в стакан. Что наблюдаете?
Составьте отчет, заполнив таблицу.
Опыт №3 Взаимодействие хлорида аммония с гидроксидом натрия.
Положите в пробирку немного хлорида аммония. Налейте в пробирку столько раствора гидроксида натрия, чтобы хлорид аммония покрылся ним. Тщательно встряхните. Осторожно понюхайте содержимое пробирки.
Составьте отчет, заполнив таблицу.
Опыт №4 Взаимодействие сульфата меди (II) с гидроксидом натрия.
Налейте в пробирку 2 мл раствора гидроксида натрия, а затем добавьте в неё 2-3 капли сульфата меди (II). Что наблюдаете?
Составьте отчет, заполнив таблицу.
Опыт №5 Взаимодействие гидроксида меди (II) с соляной кислотой.
К гидроксиду меди (II) прилейте немного раствора соляной кислоты. Осторожно встряхните. Что наблюдаете?
Составьте отчет, заполнив таблицу.
Опыт №6 Горение спирта
Налейте в чашку 2 мл этилового спирта. Осторожно подожгите его. Что наблюдаете? Составьте отчет, заполнив таблицу.
Опыт №7 Разложение малахита
Насыпьте в пробирку небольшое количество малахита. Нагрейте его в пламени спиртовки. Что наблюдаете?
Составьте отчет, заполнив таблицу.
|
Что делали |
Наблюдения |
Выводы (признак химической реакции) |
|
Опыт №1 |
||
|
Опыт №2 |
||
|
Опыт №3 |
||
|
Опыт №4 |
||
|
Опыт №5 |
||
|
Опыт №6 |
||
|
Опыт №7 |
Практическая работа № 6
по теме: «Свойства кислот, оснований, оксидов и солей»
Цель: осуществить на практике реакции, характеризующие свойства кислот, оснований, оксидов и солей.
Оборудование и реактивы: штатив с пробирками; серная кислота [H2SO4], фосфорная кислота [H3PO4], цинк [Zn], железо [Fe], оксид меди (II) [CuO], гидроксид натрия [NaOH], нитрат серебра [AgNO3], хлорид бария [BaCl2], карбонат натрия [Na2CO3], фосфат натрия [Na3PO4], хлорид меди (II) [CuCl2], фенолфталеин.
Инструктаж по технике безопасности:
Ход работы
|
Что делали |
Наблюдения и уравнения химических реакций |
|
Опыт 1 |
|
|
а) |
|
|
б) |
|
|
в) |
|
|
г) |
|
|
Опыт 2 |
|
|
а) |
|
|
б) |
|
|
в) |
|
|
г) |
Порядок выполнения работы
Опыт 1. Осуществите реакции, характеризующие свойства раствора серной кислоты:
а) кислота + металл = соль + H2↑
б) кислота + основный оксид = соль + Н2О
в) кислота + основание = соль + Н2О
г) кислота + соль = соль + кислота
Составьте уравнения проделанных реакций в молекулярном и ионном виде.
Опыт 2. Проделайте реакции, характеризующие свойства хлорида меди (II):
а) соль + металл = соль + металл
б) соль + щелочь = основание ↓ + соль
в) соль + кислота = соль + кислота
г) соль + соль = соль + соль↓
Составьте уравнения проделанных реакций в молекулярном и ионном виде.
Практическая работа № 7
по теме: «Решение экспериментальных задач»
Цель: экспериментальным путем осуществить поставленные задачи.
Оборудование и реактивы: штатив с пробирками; сульфат меди (II) [CuSO4], гидроксид натрия [NaOH], хлорид бария [BaCl2], сульфат натрия [Na2SO4], сульфат магния [MgSO4], карбонат натрия [Na2CO3], соляная кислота [HCl], фенолфталеин.
Инструктаж по технике безопасности
Ход работы
|
Что делали |
Наблюдения и уравнения химических реакций |
Вывод о типе химической реакции |
|
Опыт 1. |
||
|
а) |
||
|
б) |
||
|
в) |
||
|
Опыт 2. |
||
|
а) |
||
|
б) |
Порядок выполнения работы
Опыт 1. Осуществите реакции, схемы которых даны:
а) Ba2+ + SO42- = BaSO4
б) CO32- + 2H+ = H2O + CO2↑
в) ОН— + Н+ = Н2О
В таблицу запишите наблюдения и уравнения реакций в молекулярном полном и сокращенном и ионном виде.
Опыт 2. Пользуясь растворами, находящимися на столе, получите:
а) гидроксид меди (II)
б) карбонат магния
Наблюдения запишите в таблицу. Составьте уравнения реакций в молекулярном, полном и сокращенном ионном виде.
Инструкции
для
выполнения практических работ
по
химии
для
обучающихся 8 классов общеобразовательных
учреждений
(базовый
уровень)
УМК
О.С.Габриелян
Составила
учитель
химии
ГБОУ
«Школа № 15 имени М. С. Батраковой
г.
о. Енакиево»
Толстолуцкая
Елена Ивановна
Практическая
работа № 1
«Правила
работы в лаборатории и приёмы обращения
с лабораторным оборудованием»
Цель
работы:
изучить правила техники безопасности
при работе в химическом кабинете, приемы
обращения с лабораторным оборудованием,
строение пламени.
Реактивы
и оборудование:
лабораторный штатив с лапкой и кольцом,
спиртовка, спички, лабораторная посуда.
Ход
работы
1
Инструктаж по ТБ в кабинете химии.
2
Выполнение практической части работы.
Опыт
1
Знакомство с лабораторным оборудованием
и его назначением.
Опыт
2
Приемы обращения с лабораторным штативом
Лабораторный
штатив служит для закрепления оборудования
во время опытов. Измените положение
лапки и кольца штатива, ослабив винты
и передвинув муфты вдоль стержня.
Закрепите в лапке пробирку вертикально,
затем горизонтально. Помните, что крепко
зажатая пробирка может лопнуть! Сделайте
в тетради рисунок лабораторного штатива.
Подпишите
Опыт
3
Приемы обращения со спиртовкой и изучение
строения пламени.
Зажгите
спиртовку. Изучите части, из которых
состоит пламя. Отметьте цвет пламени.
Потушите спиртовку, накрыв пламя
колпачком. Сделайте в тетради рисунок
спиртовки. Подпишите ее части. Сделайте
рисунок пламени, указав цвет и температуру
пламени.
3
Оформление работы. В тетради для
практических работ начертите таблицу:
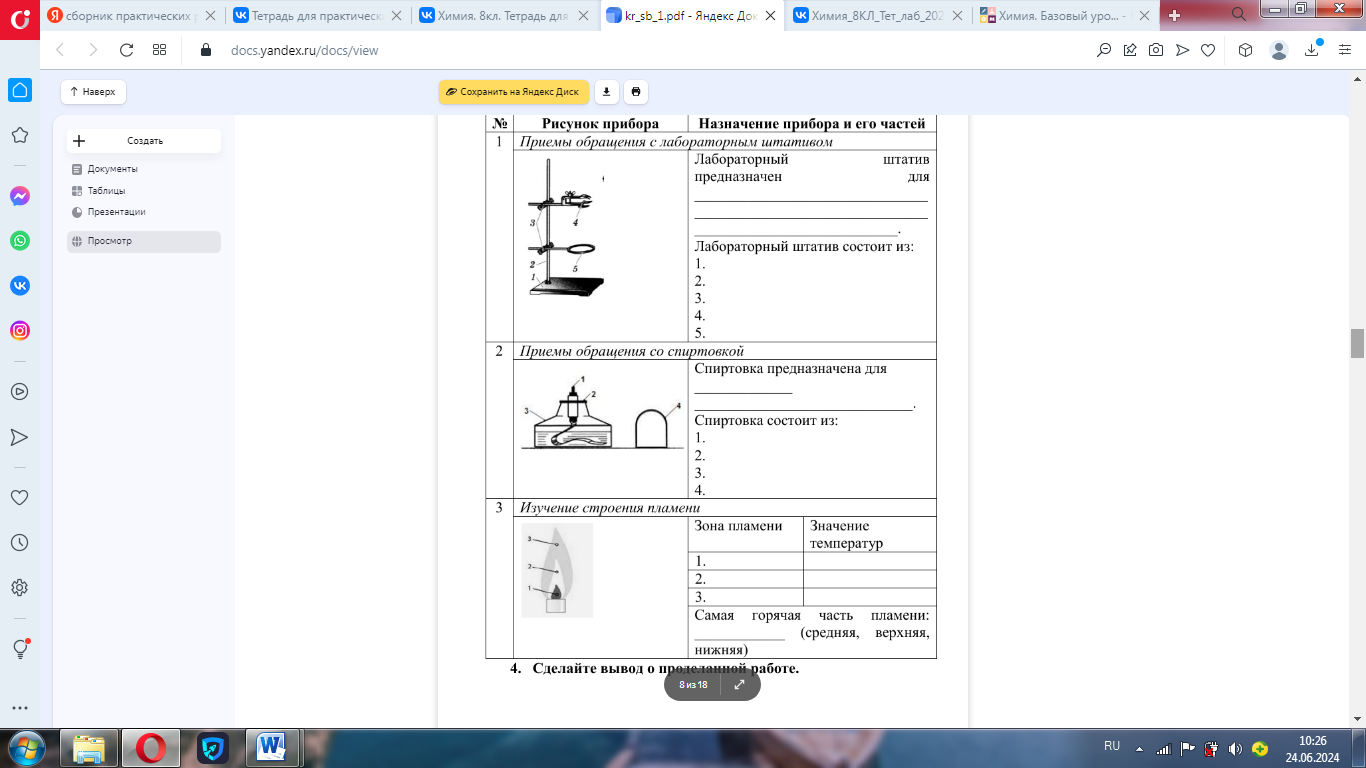
4.
Сделайте вывод о проделанной работе.
Практическая
работа № 2
«Разделение
смесей (на примере очистки поваренной
соли)»
Цель
работы:
изучить простейшие способы очистки
веществ: растворение в воде, фильтрование,
выпаривание.
Реактивы
и оборудование:
спиртовка с поставкой для чаши, спички,
смесь поваренной соли с
песком,
воронка для фильтрования, два химических
стакана, вода, фильтровальная бумага,
фарфоровая чашка для выпаривания,
стеклянная палочка.
Ход
работы
1
Инструктаж по ТБ в кабинете химии.
2
Выполнение практической части работы.
Опыт
1
Растворение в воде
В
стакан со смесью поваренной соли и песка
добавьте воды до половины стакана.
Содержимое стакана перемешайте стеклянной
палочкой. Отметьте изменения, произошедшие
в стакане. Сделайте вывод, для разделения
каких веществ можно применять операцию
растворения в воде.
Опыт
2
Фильтрование
Сложите
бумажный фильтр и поместите в воронку
для фильтрования, предварительно смочив
несколькими каплями воды. Установите
воронку с фильтром на горлышко колбы,
в которую
будет
собираться очищенный раствор (фильтрат).
Медленно тонкой струйкой налейте на
фильтр немного мутного раствора,
полученного в опыте 1. Дождитесь, пока
в колбе соберется
фильтрат.
Отметьте изменения, происходящие на
фильтре. Сделайте вывод, для каких целей
можно применять операцию фильтрования.
Опыт
3
Выпаривание
В
подставку для спиртовки установите
фарфоровую чашку для выпаривания и
поместите в нее 1 мл фильтрата. Зажгите
спиртовку и продолжайте нагревание до
полного испарения жидкости на предметном
стекле. Отметьте изменения, происходящие
на предметном стекле. Сделайте вывод,
для каких целей можно применять операцию
выпаривания.
3.
Оформление работы
Результаты
выполнения работы записывают в таблицу:
|
№ и |
Что |
Что |
Выводы |
4.
Сделайте общий вывод о выполненной
работе.
5.
Выполните тестовые задания
1.
Отличие морской соли от поваренной в
том, что первая:
А)
не растворяется в воде; Б) не солёная
на вкус; В) содержит много примесей;
Г) другое химическое вещество.
2.
Какими физическими свойствами не
обладает соль?
А)
солёная; Б) плохо растворяется в воде;
В) имеет белый цвет; Г) сыпучий порошок.
3.
Какой метод можно использовать для
очистки поваренной соли?
А)
фильтрование; Б) кристаллизация; В)
выпаривание; Г) хроматография.
4.
Какую смесь можно разделить методом
фильтрования?
А)
сахара и песка; Б) соли и сахара; В)
железных опилок и древесной стружки;
Г) бензина и воды.
5.
Что из перечисленного является эмульсией?
А)
растительное масло; Б) раствор соли;
В) майонез; Г) чай.
Практическая
работа № 3
«Получение
и собирание кислорода, изучение его
свойств»
Цель
работы:
получить кислород методом вытеснения
воздуха и методом вытеснения водой и
изучить его свойства.
Реактивы
и оборудование:
пероксид водорода, оксид марганца,
лучина, пробка с газоотводной трубкой,
лучинка, спиртовка, спички, химический
стакан, вата, пробирка.
Ход
работы:
1
Инструктаж по ТБ в кабинете химии.
2
Оформление практической работы:
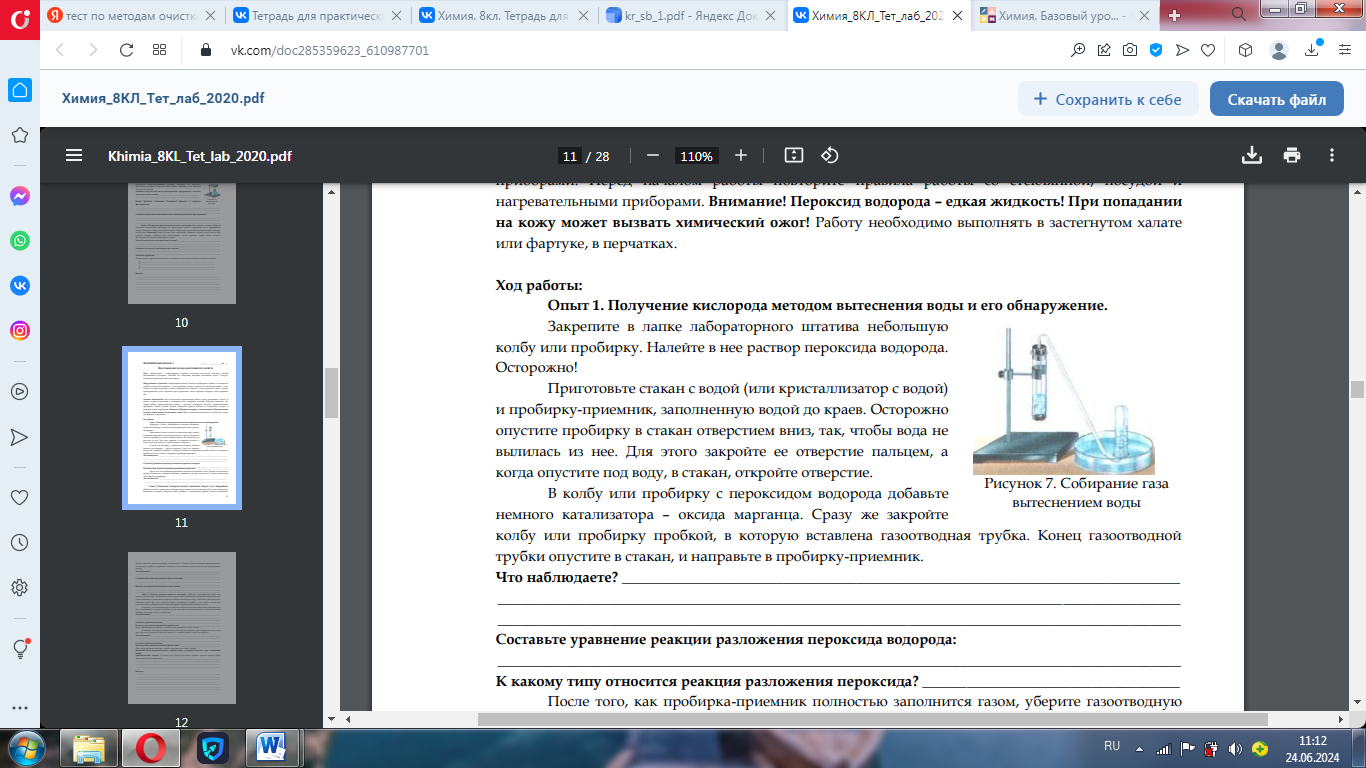
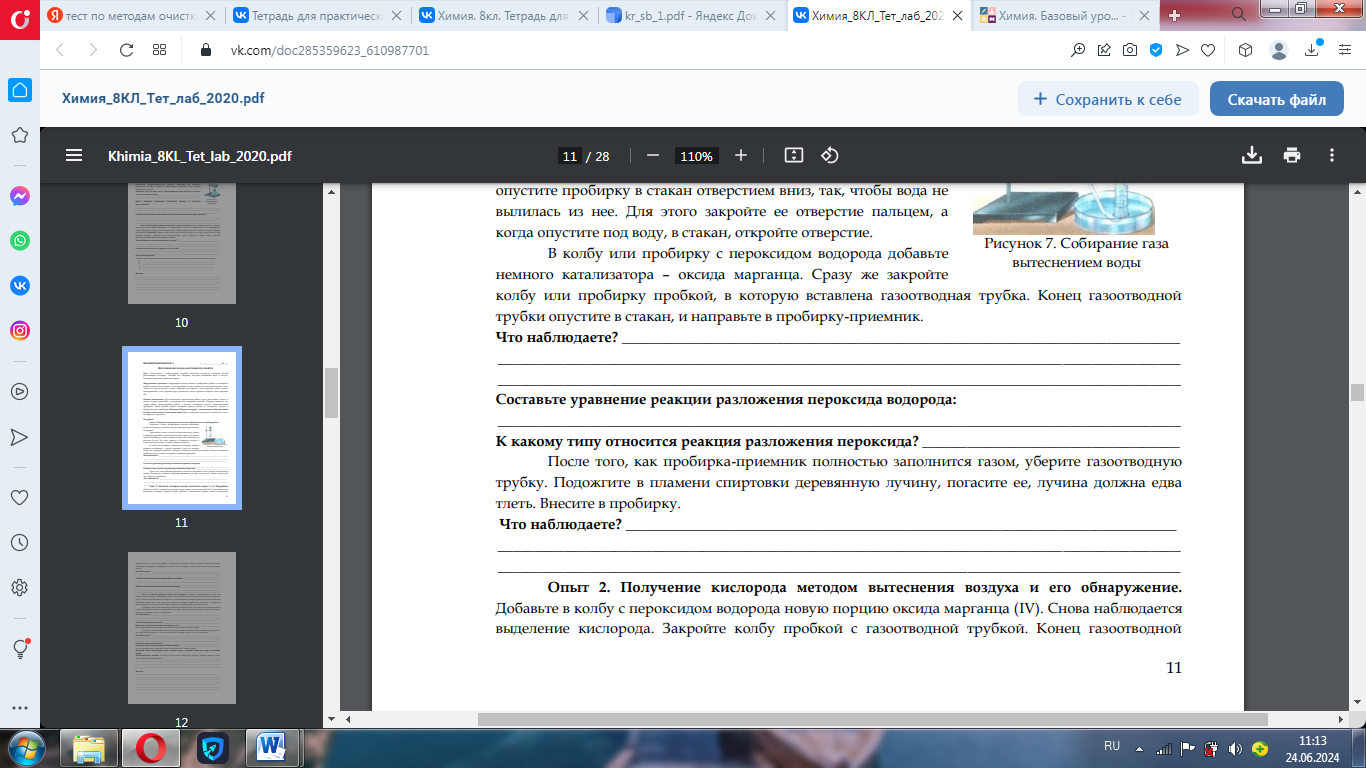
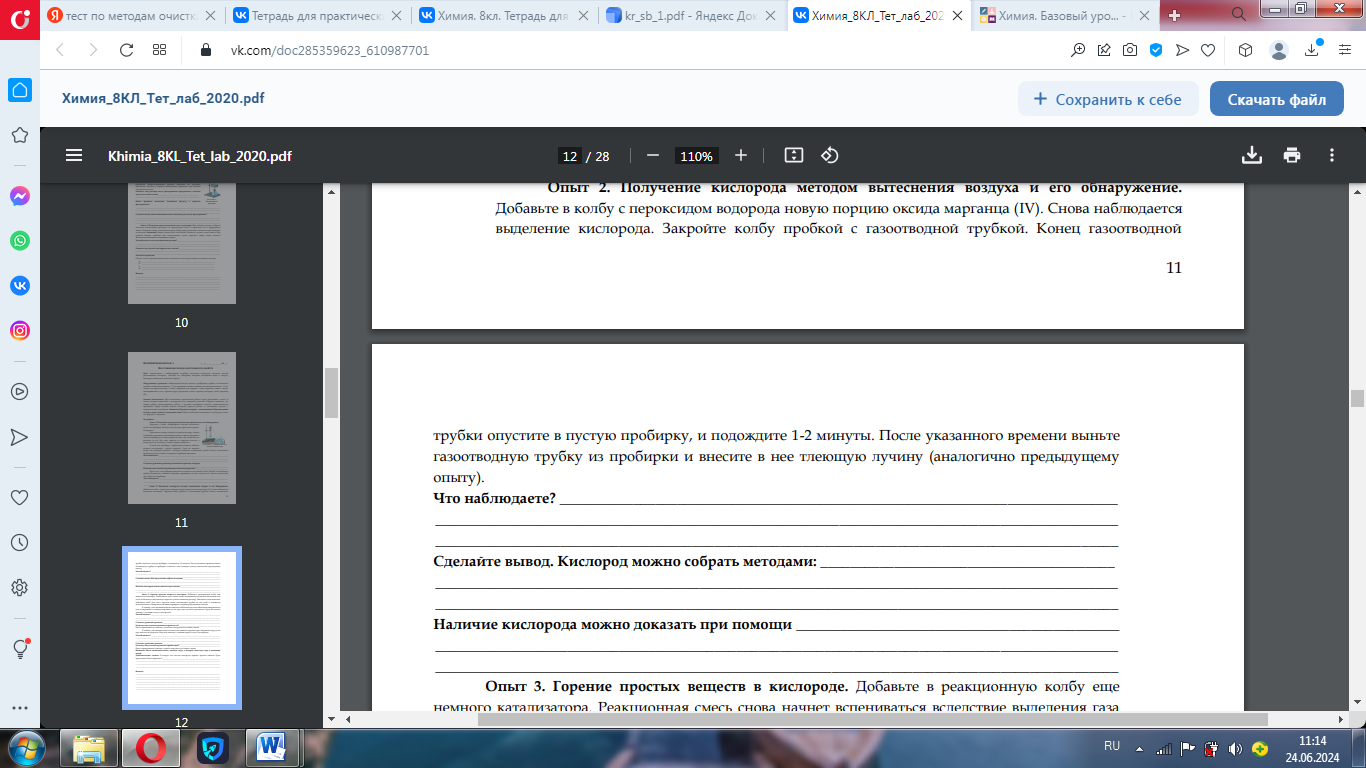
3.
Оформление работы
Результаты
выполнения работы записывают в таблицу:
|
№ и |
Что |
Что |
Выводы |
4.
Сделайте вывод о проделанной работе,
ответив на вопросы:
1
Из каких веществ получают кислород в
лаборатории? 2 Как доказать, что полученный
газ — кислород? 3 Какие вещества называются
катализаторами?
Практическая
работа № 4
«Получение
и собирание водорода, изучение его
свойств»
Цель:
получить водород в лаборатории и изучить
его свойства.
Оборудование
и реактивы:
цинк, соляная кислота, лучина, спички,
газоотводная трубка, две пробирки,
штатив.
Ход
работы:
1
Инструктаж о правилах техники безопасности.
2
Выполнение практической работы.
Опыт
№ 1
Получение водорода реакцией замещения
между цинком и соляной кислотой.
В
пробирку опустите 2-3 гранулы цинка.
Налейте
соляной кислоты (столько, чтобы кислота
лишь покрывала цинк) и закройте пробкой
с газоотводной трубкой. Газоотводную
трубку накройте чистой пробиркой.
Пронаблюдайте
за происходящим в пробирке.
Опыт
№ 2
Изучение физических свойств водорода.
Рассмотрите
пробирку с собранным водородом и отметьте
его физические свойства: агрегатное
состояние, цвет, запах, растворимость
в воде, плотность по отношению к воздуху.
Запишите
название опыта, ваши наблюдения и
соответствующий вывод.
Опыт
№ 3
Проверка водорода на чистоту.
Для
опыта используется водород, собранный
вытеснением воздуха. Не изменяя положения
пробирки приемника, поднесите ее вплотную
к пламени горелки или спички и резко
поверните так, чтобы ее отверстие
оказалось в пламени. Если при этом
раздается резкий “лающий” звук, с газом
(водородом) работать нельзя, так как он
содержит примесь воздуха. Необходимо
некоторое время подождать, пока из
пробирки будет вытеснен весь воздух.
Если вы услышите легкий звук, напоминающий
“п-пах”, с водородом можно работать.
Запишите название опыта, ваши наблюдения
и соответствующий вывод.
3.
Оформление в виде таблицы:
|
№ и |
Что |
Что |
Уравнения |
|
|||
|
|||
|
4.Сделайте
вывод о проделанной работе.
5.
Выполните тестовые задания.
1.
Агрегатное
состояние водорода при нормальных
условиях
а)
жидкость б) твердое вещество
в) газ
2.
Формула
простого вещества водорода
а)
Н3
б) Н 2
в) Н
3.
Водород
в лаборатории получают реакцией
а)
Zn + HCl б) CH4 +
H2O
в) H2O
+ C
4.Группа,
в которой находится водород
а)
3 б) 2
в) 1
5.
Порядковый
номер водорода
а)
1 б) 2
в) 3
Практическая
работа № 5
«Приготовление
растворов с определённой массовой долей
растворённого вещества»
Цель:
применение приобретенных навыки по
решению задач на приготовление растворов
для приготовления раствора с определенной
массовой концентрацией; продолжить
формировать навыки обращения с
лабораторным оборудованием, посудой,
химическими реактивами.
Оборудование
и реактивы:
весы, стаканы, стеклянная палочка,
шпатель, мерный цилиндр или мензурка,
хлорид натрия.
Ход работы:
1
Инструктаж о правилах техники безопасности.
2
Выполнение практической работы.
Шаг 1.
Рассчитайте массу хлорида натрия и
объем воды, необходимые для приготовления
раствора массой ____________ г, с массовой
долей растворенной соли ___________% (данные
для задачи указывает учитель).
Дано:
m(раствора)
= г Решение:
ω (NaCl) = %
Ответ:
m(NaCl) — ? V(H2O) — ?
Шаг 2.
При помощи весов взвесьте рассчитанное
количество хлорида натрия. Навеску соли
аккуратно перенесите в стакан.
Шаг 3.
Отмерьте необходимый объем воды при
помощи мерного цилиндра или мензурки.
Шаг 4.Прилейте
отмеренный объем воды к навеске соли в
стакане. Размешайте смесь палочкой до
полного растворения соли.
3 Сделайте
вывод о проделанной работе.
4. Ответьте
на контрольные вопросы:
1). Какое
вещество называют растворителем?
2). Как изменится
массовая доля приготовленного вами
раствора, если его разбавить водой в
два раза?
3). Какие
растворы называются насыщенными?
Практическая
работа № 6.
Решение
экспериментальных задач по теме «Основные
классы неорганических соединений»
Цель:
закрепить знания об основных классах
неорганических соединений, научиться
решать экспериментальные задачи.
Оборудование
и реактивы:
магний, оксид магния, растворы: HCl, NaOH,
CuSO4; индикаторы, пипетка, стеклянная
палочка.
Ход
работы:
1
Инструктаж по правилам ТБ при работе в
кабинете химии.
2
Ознакомьтесь с заданием:
Задание
1
В двух пробирках находятся растворы: в
1 – раствор соляной кислоты, во 2-
гидроксида натрия. Как опытным путем
определить, в какой пробирке находится
каждое из веществ?
Задание
2
В вашем распоряжении есть магний, оксид
магния и кислоты. Получить хлорид магния.
Задание
3
Осуществите превращения по схеме: CuSO4
→ Cu(OH)2.
3
Выполните необходимые опыты.
4
Результаты проведенной работы оформите
в виде таблицы:
|
№ опыта |
Что |
Что |
Уравнения |
|
|
Стеклянной полоску индикатора пробирок, приливаем |
||
|
|
соляной опускаем немного |
||
|
|
сульфата |
5
После проведения практической работы
сделайте общий вывод.
